题目内容
12.如图,A、B、C、D、E是长式元素周期表中的5种元素(不包括镧系和锕系).下列说法不正确的是( )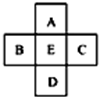
| A. | A、E原子序数之差可能为2 | B. | D、E原子序数之差可能是8、18或32 | ||
| C. | B、C原子序数之差一定是2 | D. | B、D原子序数之差不可能是7 |
分析 由五种元素在周期表中的位置可知,A至少应处于第二周期,最多处于第五周期,若A处于第二周期,那么E处于第三周期,那么A、E至少相差8,以此解答该题.
解答 解:A.A不可能处于第一周期,故A、E原子序数之差不可能是2,故A错误;
B.若A处于第二周期,那么E处于第三周期,D处于第四周期,那么E、D相差18,若E为第五周期,那么E、D相差32,故B正确;
C.B、C处于同一周期,那么B、C原子序数之差一定是2,故C正确;
D.由以上分析可知BD可能相差19或33,故不可能相差7,故D正确,
故选A.
点评 本题考查位置结构与性质的关系,题目难度不大,本题注意把握元素周期表的结构特点,为常考查的知识,注意把握元素周期表的组合规律.

练习册系列答案
相关题目
2.25℃时,几种弱酸的电离常数如下:
25℃时,下列说法正确的是( )
| 弱酸的化学式 | CH3COOH | HCN | H2S |
| 电离常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=1.3×10-7 K2=7.1×10-15 |
| A. | 等物质的量浓度的各溶液PH关系为:PH(Na2S)>PH(NaCN)>PH(CH3COONa) | |
| B. | a mol/LHCN溶液与b mol/LNaOH溶液等体积混合,所得溶液中c(Na+)>c(CN-),则a一定大于b | |
| C. | NaHS和Na2S的混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HS-)+c(S2-) | |
| D. | 某浓度的NaCN溶液的pH=d,则其中由水电离出的c(H+)=10-dmol/L |
3.下列溶液:①pH=0的盐酸;②0.5mol/L的盐酸溶液;③0.1mol/L的氯化铵溶液;④0.1mol/L的氢氧化钠溶液;⑤0.1mol/L的氟化钠溶液,由水电离的c(H+)由大到小的顺序正确的是( )
| A. | ①②③④⑤ | B. | ③⑤④②① | C. | ①②③⑤④ | D. | ⑤③④①② |
20.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 9g甲基(-CH3)所含有的电子数是10 NA个 | |
| B. | 22.4L乙烷中含有的共价键数为7NA个 | |
| C. | 常温下,14g乙烯和丙烯的混合物中总原子数为3NA个 | |
| D. | 4.2g C3H6中含有的碳碳双键数一定为0.1NA |
7.二元酸H2A在水中发生电离:H2A═H++HA-和HA-?H++A2-,则下列几种物质的水溶液中关系式不正确的是( )
| A. | NaHA:c(Na+)>c(HA-)>c(OH-)>c(H+) | B. | NaHA:c(Na+)=c(A2-)+c(HA-) | ||
| C. | Na2A:c(Na+)>c(A2-)>c(OH-)>c(H+) | D. | H2A:c(H+)=c(HA-)+2c(A2-)+c(OH-) |
1.在氧气中充分灼烧1.20g S和Fe组成的化合物,使其中的S全部转化为SO2,将这些SO2与Cl2反应全部转化为H2SO4,共消耗标况下氯气0.44L,则原化合物中S的质量分数为( )
| A. | 53% | B. | 46% | C. | 18% | D. | 36% |
2.已知R2+离子核外有a个电子,b个中子.表示R原子组成正确的是( )
| A. | ${\;}_{a}^{b}$ R | B. | ${\;}_{a-2}^{a+b-2}$ R | C. | ${\;}_{a+2}^{a+b+2}$ R | D. | ${\;}_{a-2}^{a+b}$ R |
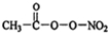 (PAN)等二次污染物.
(PAN)等二次污染物.