题目内容
18.下列有关物质的性质或结构的说法中正确的是( )| A. | L层上的电子数为奇数的原子不一定是主族元素的原子 | |
| B. | 只由共价键形成的物质不一定是共价化合物 | |
| C. | 化学键的形成一定伴随着电子的转移和能量变化 | |
| D. | 元素周期表中,位于金属和非金属分界线附近的元素属于过渡元素 |
分析 A.原子的L层上的电子数为奇数的元素,说明L层为填充满电子,元素为锂、硼、氮、氟;
B、仅由共价键形成的化合物是共价化合物;
C、化学键的形成一定伴随着能量的变化,但不一定有电子转移;
D.元素周期表中位于金属和非金属分界线附近的元素属于半导体元素.
解答 解:A.L层电子为奇数的所有元素为锂、硼、氮、氟,均为主族元素,故A错误;
B、仅由共价键形成的化合物是共价化合物,而不是物质,物质可能是单质,如氢气分子中存在氢氢共价键,但不是化合物,故B正确;
C、化学键的形成一定伴随着能量的变化,但不一定有电子转移,故C错误;
D.元素周期表中位于金属和非金属分界线附近的元素属于半导体元素,而不是过渡元素,故D错误;
故选B.
点评 本题考查元素周期律,题目难度不大,熟悉元素在周期表中的位置及元素的性质即可解答,注意同期表中的特殊元素.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
6.草酸是一种重要的试剂.下面是利用草酸探究浓度对反应速率影响的实验.
(1)为证明浓度对反应速率的影响,曾有教科书《化学反应原理》设计了如下实验:取两支试管,各加入4mL0.01mol•L-1的KMnO4酸性溶液,分别向其中加入0.1mol•L-1、0.2mol•L-1 H2C2O4溶液2mL,记录溶液褪色所需时间.
实验中发生反应的离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;
预期现象是:
①溶液的颜色由紫色变为无色,
②其中加入0.2mol•L-1H2C2O4的那支试管中的溶液先变色.
然而实验结果并不尽如人意.实验过程颜色复杂,且褪色先缓慢,后逐渐加快;最大的问题是草酸浓度大,反应速率却更慢.
本实验能否作为课堂实验研究浓度对化学反应速率的影响?适宜的条件是怎样的?某校一研究小组对此进行了探究.下面是他们的实验报告的一部分:
表1 试验安排及结果
应用SPSS16.0对正交试验结果进行方差分析,结果如表
表2 各因素水平的数据处理结果
(2)由表2可知,三因素中,C的浓度(选填“A、B或C”,下空同)对反应速率影响显著,而A和B的浓度对反应速率的影响不显著.
(3)由表2可知,当高锰酸钾浓度为0.005mol•L-1、草酸浓度为0.1mol•L-1时,反应最快.即因素A、B的较适宜实验条件得以确定.
根据以上实验结果,该小组同学继续探究硫酸的浓度是怎样影响本反应速率的,测得如下实验结果:
表3 不同硫酸浓度下的褪色时间
(4)根据课堂实验的合适时间,可选溶液的褪色时间约为1分钟和2分钟的两份溶液,即此时硫酸的浓度为18mol•L-1和10mol•L-1,这也有利于观察这两个反应速率的差异.
结论:草酸与酸性高锰酸钾溶液的反应,可作为课堂实验探究浓度对反应速率的影响.
(1)为证明浓度对反应速率的影响,曾有教科书《化学反应原理》设计了如下实验:取两支试管,各加入4mL0.01mol•L-1的KMnO4酸性溶液,分别向其中加入0.1mol•L-1、0.2mol•L-1 H2C2O4溶液2mL,记录溶液褪色所需时间.
实验中发生反应的离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;
预期现象是:
①溶液的颜色由紫色变为无色,
②其中加入0.2mol•L-1H2C2O4的那支试管中的溶液先变色.
然而实验结果并不尽如人意.实验过程颜色复杂,且褪色先缓慢,后逐渐加快;最大的问题是草酸浓度大,反应速率却更慢.
本实验能否作为课堂实验研究浓度对化学反应速率的影响?适宜的条件是怎样的?某校一研究小组对此进行了探究.下面是他们的实验报告的一部分:
表1 试验安排及结果
| 实验 编号 | A(KMnO4溶液浓度/mol•L-1) | B(草酸溶液浓度/mol•L-1) | C(硫酸溶液浓度/mol•L-1) | 褪色时间/s |
| 1 | 3 | 3 | 1 | 336 |
| 2 | 1 | 2 | 3 | 82 |
| 3 | 3 | 1 | 3 | 76 |
| 4 | 1 | 3 | 2 | 133 |
| 5 | 2 | 3 | 3 | 102 |
| 6 | 3 | 2 | 2 | 156 |
| 7 | 2 | 2 | 1 | 300 |
| 8 | 2 | 1 | 2 | 115 |
| 9 | 1 | 1 | 1 | 200 |
表2 各因素水平的数据处理结果
| A(KMnO4溶液) | B(草酸溶液) | C(硫酸溶液) | |||||||
| 浓度/mol•L-1 | 0.005 | 0.010 | 0.015 | 0.1 | 0.5 | 0.9 | 6 | 12 | 18 |
| 平均褪色时间/s | 138.3 | 172.3 | 189.3 | 130.3 | 179.3 | 190.3 | 278.7 | 134.7 | 86.7 |
(3)由表2可知,当高锰酸钾浓度为0.005mol•L-1、草酸浓度为0.1mol•L-1时,反应最快.即因素A、B的较适宜实验条件得以确定.
根据以上实验结果,该小组同学继续探究硫酸的浓度是怎样影响本反应速率的,测得如下实验结果:
表3 不同硫酸浓度下的褪色时间
| c(H2SO4)/mol•L-1 | 18 | 16 | 14 | 12 | 10 | 8 | 6 |
| 褪色时间/s | 67 | 83 | 90 | 103 | 129 | 146 | 200 |
结论:草酸与酸性高锰酸钾溶液的反应,可作为课堂实验探究浓度对反应速率的影响.
13.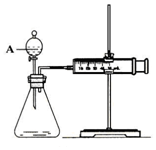 用如图所示的装置来测定镁与硫酸反应的速率,在锥形瓶中加入0,7克镁带,按图连接好装置,从A中加入20.0ml0.5mol/LH2SO4.记录注射器活塞的位置和相应的时间.记录数据如表
用如图所示的装置来测定镁与硫酸反应的速率,在锥形瓶中加入0,7克镁带,按图连接好装置,从A中加入20.0ml0.5mol/LH2SO4.记录注射器活塞的位置和相应的时间.记录数据如表
(1)检查该装置气密性的方法是将装置安装好后,关闭分液漏斗活塞,将注射器活塞拉出一定距离,然后松开活塞,若活塞回到原位则气密性良好;或先将活塞位置固定好,然后从分液漏斗中加水,若水不能顺利流下,则装置气密性好.
(2)仪器A的名称是分液漏斗.
(3)0-t时间段与t-2t时间段,化学反应速率最快的是t-2t,原因是镁与硫酸反应放热,温度升高,反应速率加快.
(4)用上述装置探究Fe3+、Cu2+对双氧水分解速率的影响,所用试剂:5%H2O2、0,1mol/LFeCl3、0.2mol/LCuCl2,完成表的实验设计:
①写出本实验H2O2分解反应方程式并标明电子转移的方向和数目: .
.
②上表中需要添加的物质是4mlFeCl3溶液.
③本实验需要测定的数据是收集相同体积的氧气所需时间(或相同时间产生氧气的体积).
(5)为确定MnO2催化双氧水分解的最佳条件,用该实验装置进行实验,反应物用量和反应停止的时间数据如表.
分析表中数据回答下列问题:
①相同浓度的过氧化氢的分解速率随着MnO2用量的增加而加快(填“加快”、“减慢”或“不变”).
②从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入0.3 g的MnO2为较佳选择.
③该小组的某同学分析上述数据后认为:“当用相同质量的MnO2时,双氧水的浓度越小,所需要的时间就越少,亦即其反应速率越快”的结论,你认为是否正确?不正确(填“正确”或“不正确”),理由是H2O2的浓度扩大二倍(从1.5%-→3.0%),但反应所需时间比其二倍小的多.(提示:H2O2溶液的密度可认为近似相等.)
 用如图所示的装置来测定镁与硫酸反应的速率,在锥形瓶中加入0,7克镁带,按图连接好装置,从A中加入20.0ml0.5mol/LH2SO4.记录注射器活塞的位置和相应的时间.记录数据如表
用如图所示的装置来测定镁与硫酸反应的速率,在锥形瓶中加入0,7克镁带,按图连接好装置,从A中加入20.0ml0.5mol/LH2SO4.记录注射器活塞的位置和相应的时间.记录数据如表| 时间/s | 0 | t | 2t | … |
| 活塞的位置/ml | 17.3 | 25.6 | 36.6 | … |
(2)仪器A的名称是分液漏斗.
(3)0-t时间段与t-2t时间段,化学反应速率最快的是t-2t,原因是镁与硫酸反应放热,温度升高,反应速率加快.
(4)用上述装置探究Fe3+、Cu2+对双氧水分解速率的影响,所用试剂:5%H2O2、0,1mol/LFeCl3、0.2mol/LCuCl2,完成表的实验设计:
| 实验序号 | 双氧水体积/mL | 蒸馏水体积/mL | 添加的物质 |
| 1 | 10 | 0 | 4mLFeCl3 |
| 2 | 10 | 2 | 2mLCuCl2 |
 .
.②上表中需要添加的物质是4mlFeCl3溶液.
③本实验需要测定的数据是收集相同体积的氧气所需时间(或相同时间产生氧气的体积).
(5)为确定MnO2催化双氧水分解的最佳条件,用该实验装置进行实验,反应物用量和反应停止的时间数据如表.
 | 0.1g | 0.3g | 0.8g |
| 10mL1.5% | 223s | 67s | 36s |
| 10mL3.0% | 308s | 109s | 98s |
| 10mL4.5% | 395s | 149s | 116s |
①相同浓度的过氧化氢的分解速率随着MnO2用量的增加而加快(填“加快”、“减慢”或“不变”).
②从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入0.3 g的MnO2为较佳选择.
③该小组的某同学分析上述数据后认为:“当用相同质量的MnO2时,双氧水的浓度越小,所需要的时间就越少,亦即其反应速率越快”的结论,你认为是否正确?不正确(填“正确”或“不正确”),理由是H2O2的浓度扩大二倍(从1.5%-→3.0%),但反应所需时间比其二倍小的多.(提示:H2O2溶液的密度可认为近似相等.)
3.关于下列关于周期表的描述正确的是( )
| A. | 副族元素中没有非金属 | |
| B. | 除短周期外,其他周期均有18种元素 | |
| C. | ⅠA族的所有元素都为金属元素 | |
| D. | 同周期ⅡA族与ⅢA族元素原子序数相差只有1、11 |
10.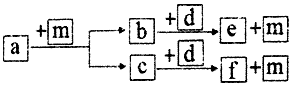 短周期元素W、X、Y、Z的原子序数依次递增,a、b、c、d、e、f是由这些元素组成的化合物,d是淡黄色粉末,m为元素Y的单质,通常为无色无味的气体.上述物质的转化关系如图所示.下列说法错误的是( )
短周期元素W、X、Y、Z的原子序数依次递增,a、b、c、d、e、f是由这些元素组成的化合物,d是淡黄色粉末,m为元素Y的单质,通常为无色无味的气体.上述物质的转化关系如图所示.下列说法错误的是( )
 短周期元素W、X、Y、Z的原子序数依次递增,a、b、c、d、e、f是由这些元素组成的化合物,d是淡黄色粉末,m为元素Y的单质,通常为无色无味的气体.上述物质的转化关系如图所示.下列说法错误的是( )
短周期元素W、X、Y、Z的原子序数依次递增,a、b、c、d、e、f是由这些元素组成的化合物,d是淡黄色粉末,m为元素Y的单质,通常为无色无味的气体.上述物质的转化关系如图所示.下列说法错误的是( )| A. | 简单离子半径:Z>Y | |
| B. | Z2Y2中既含有离子键又含有共价键,其中阳离子和阴离子的比值为2:1 | |
| C. | 简单气态氢化物的热稳定性:Y>X | |
| D. | 由上述4种元素组成的化合物属于离子化合物 |
7.下列离子在指定溶液中一定能大量共存的是( )
| A. | 能使甲基橙变红的溶液中:Fe2+、Al3+、NO3-、Cl- | |
| B. | 在pH=12的溶液中:Na+、AlO2-、NO3-、S2- | |
| C. | 室温下,由水电离的c(H+)=10-10mol/L的溶液中:Cl-、HCO3-、NO3-、NH4+ | |
| D. | 加入Mg能放出H2的溶液中:Mg2+、NH4+、ClO-、K+ |
8.关于小苏打溶液的表述错误的是( )
| A. | c(Na+)═c(HCO3-)+c(CO32-)+c(H2CO3) | B. | c(Na+)+c(H+)═c(HCO3-)+2c(CO32-)+c(OH-) | ||
| C. | HCO3-的电离程度小于其水解程度 | D. | c(Na+)>c(HCO3-)>c(OH-)>c(CO32-)>c(H+) |
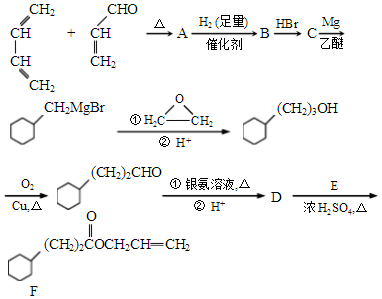
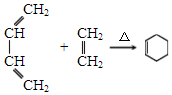
 ,A中所含官能团的名称是醛基、碳碳双键.
,A中所含官能团的名称是醛基、碳碳双键. .
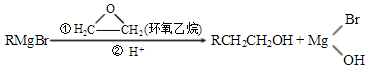
.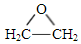 )为原料制备1丁醇,设计合成路线
)为原料制备1丁醇,设计合成路线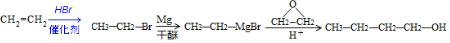 (其它试剂任选).(合成路线常用表示方法为:A $→_{反应条件}^{反应试剂}$ B …$→_{反应条件}^{反应试剂}$目标产物)
(其它试剂任选).(合成路线常用表示方法为:A $→_{反应条件}^{反应试剂}$ B …$→_{反应条件}^{反应试剂}$目标产物)