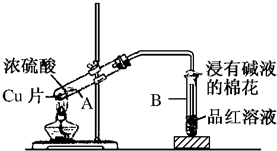
题目内容
11.W、X、Y、Z为短周期内除稀有气体外的4种元素,它们的原子序数依次增大,其中只有Y为金属元素且其焰色反应为黄色.Y和W的最外层电子数相等.Y、Z两元素原子的质子数之和为W、X两元素质子数之和的3倍且Z的单质为淡黄色固体.由此可知:(1)写出元素符号WH,ZS.
(2)W2X的电子式为
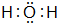 .
.(3)由Y、X、W组成的化合物中有离子键和共价键.
(4)由W、X、Y、Z四种元素组成的化合物的化学式为NaHSO4,NaHSO3;写出这两种物质之间反应的离子方程式H++HSO3-=SO2↑+H2O.
分析 W、X、Y、Z为短周期内除稀有气体外的4种元素,它们的原子序数依次增大,其中只有Y为金属元素且其焰色反应为黄色,则Y为Na;Z的单质为淡黄色固体,则Z为S元素;Y、Z两元素原子的质子数之和为W、X两元素质子数之和的3倍,则W、X的质子数之和为$\frac{11+16}{3}$=9,Y和W的最外层电子数相等,则W为H元素、X为O元素,据此解答.
解答 解:W、X、Y、Z为短周期内除稀有气体外的4种元素,它们的原子序数依次增大,其中只有Y为金属元素且其焰色反应为黄色,则Y为Na;Z的单质为淡黄色固体,则Z为S元素;Y、Z两元素原子的质子数之和为W、X两元素质子数之和的3倍,则W、X的质子数之和为$\frac{11+16}{3}$=9,Y和W的最外层电子数相等,则W为H元素、X为O元素.
(1)W为H元素,Z为S元素,故答案为:H;S;
(2)H2O的电子式为: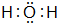 ,故答案为:
,故答案为: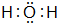 ;
;
(3)由Na、O、H组成的化合物为NaOH,含有离子键、共价键,故答案为:离子、共价;
(4)由H、O、Na、S四种元素组成的化合物为 NaHSO4、NaHSO3,这两种物质之间反应的离子方程式为:H++HSO3-=SO2↑+H2O,
故答案为:NaHSO4;NaHSO3;H++HSO3-=SO2↑+H2O.
点评 本题考查结构性质物质关系应用,元素单质的元素是推断突破口,熟练掌握元素化合物的组成与性质.

练习册系列答案
 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
1.下列物质中既有离子键又有共价键的一组是( )
| A. | NaOH、Na2O2、NH4Cl | B. | HCl、H2O、Cl2 | ||
| C. | MgCl2、NaF、KOH | D. | Xe、H2SO4、HF |
2.向盛有碘化钾溶液的试管中加入适量溴水用力振荡,再加入四氯化碳充分振荡,现象( )
| A. | 溶液呈紫色 | |
| B. | 溶液呈黄色 | |
| C. | 上层溶液接近无色,下层溶液呈紫红色 | |
| D. | 上层溶液呈紫红色,下层溶液呈无色 |
16.三种常见元素结构信息如表,试根据信息回答有关问题:
(1)C元素属于ds区,C原子的外围电子排布式:3d104s1
(2)用氢键表示式写出A的氢化物溶液中存在的所有氢键N-H…N或N-H…O或 O-H…N或O-H…O;A的氢化物分子结合一个H+形成阳离子后,其键角变大(填写“变大”、“变小”、“不变”);
(3)C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为[Cu(NH3)4]SO4,
(4)科学家通过X射线推测胆矾中微粒间的作用力,胆矾的结构示意图可简单表示如下:

则胆矾晶体中含有ABCE
A.配位键 B.离子键 C.极性共价键 D.金属键 E.氢键 F.非极性共价键
(5)下列分子结构图中的“●”表示上述相关元素的原子中除去最外层电子的剩余部分,“○”表示氢原子,小黑点“•”表示没有形成共价键的最外层电子,短线表示共价键.

在以上分子中,中心原子采用sp3杂化形成化学键是①③④(填写序号).
| 元素 | A | B | C |
| 结构信息 | 基态原子核外有两个电子层,最外层有3个未成对的电子 | 基态原子的M层有1对成对的p电子 | 基态原子核外M层全部充满,N层有一个未成对电子 |
(2)用氢键表示式写出A的氢化物溶液中存在的所有氢键N-H…N或N-H…O或 O-H…N或O-H…O;A的氢化物分子结合一个H+形成阳离子后,其键角变大(填写“变大”、“变小”、“不变”);
(3)C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为[Cu(NH3)4]SO4,
(4)科学家通过X射线推测胆矾中微粒间的作用力,胆矾的结构示意图可简单表示如下:

则胆矾晶体中含有ABCE
A.配位键 B.离子键 C.极性共价键 D.金属键 E.氢键 F.非极性共价键
(5)下列分子结构图中的“●”表示上述相关元素的原子中除去最外层电子的剩余部分,“○”表示氢原子,小黑点“•”表示没有形成共价键的最外层电子,短线表示共价键.

在以上分子中,中心原子采用sp3杂化形成化学键是①③④(填写序号).
1.在密闭容器中A与B反应生成C,其反应速率分别用v(A)、v(B)、v(C)表示.已知v(A)、v(B)、v(C)之间有以下关系:3v(B)=2v(A),2v(B)=3v(C),则此反应可表示为( )
| A. | 3A+B=C | B. | 2A+2B=3C | C. | 4A+6B=9C | D. | 9A+6B=4C |