题目内容
2.在一定条件下,RO3n-与R2-发生如下反应:RO3n-+2R2-+6H+═3R+3H2O,下列关于元素R的叙述中正确的是( )| A. | R原子的最外层上有6个电子 | B. | RO3n-中的R只能被还原 | ||
| C. | HnRO3为强酸 | D. | R的单质既有氧化性又具有还原性 |
分析 根据电荷守恒,-n+2×(-2)+6×(+1)=0,n=2,RO3n-中元素R的化合价是+4价,R是短周期元素,R2-中元素R的化合价-2价,根据元素周期律,最低负价=主族序数-8,最高正价=其族序数,且有正化合价,所以R是S元素,结合选项反应.
解答 解:根据电荷守恒,-n+2×(-2)+6×(+1)=0,n=2,RO3n-中元素R的化合价是+4价,R是短周期元素,R2-中元素R的化合价-2价,根据元素周期律,最低负价=主族序数-8,最高正价=其族序数,且有正化合价,所以R是S元素.
A.最外层上有6个电子,故A正确;
B.RO3n-中元素R的化合价是+4价,中间价态既有氧化性又有还原性,故B错误;
C、R是S元素,亚硫酸是弱酸,故C错误;
D、S的单质化合价居于中间价,既具有氧化性又具有还原性,故D正确.
故选:AD.
点评 本题考查氧化还原反应、元素化合物的性质、电荷守恒的应用等,把握发生的反应、反应中元素的化合价变化为解答的关键,侧重氧化还原反应判断的考查,题目难度不大.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
12.如图是蓝色晶体MxFey(CN)6中阴离子的最小结构单元(图中是该晶体晶胞的八分之一)下列说法正确的是( )
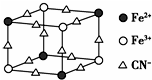

| A. | 该晶体属于离子晶体,M呈+2价 | |
| B. | 该晶体属于分子晶体,化学式为MFe2(CN)6 | |
| C. | 该晶体中与每个Fe3+距离相等且最近的CN-为12个 | |
| D. | 该晶体的一个晶胞中含有的M+的个数为4个 |
10.短周期元素X、Y、Z、W、Q的原子序数依次增大,且只有一种金属元素.其中X与W处于同一主族,Z元素原子半径在短周期中最大(稀有气体除外),W、Z之间与W、Q之间原子序数之差相等,五种元素原子最外层电子数之和为21.下列说法不正确的是( )
| A. | 气态氢化物的稳定性:Y>X>W | |
| B. | Y与Q的氢化物相遇生成白烟 | |
| C. | 气态氢化物的还原性:W>X>Y | |
| D. | Q可分别与X、Y、Z、W形成化学键类型相同的化合物 |
17.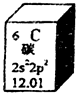 元素周期表是学习化学的重要工具,如图是元素周期表中的一格,以下对该图信息的解读中,不正确的是( )
元素周期表是学习化学的重要工具,如图是元素周期表中的一格,以下对该图信息的解读中,不正确的是( )
 元素周期表是学习化学的重要工具,如图是元素周期表中的一格,以下对该图信息的解读中,不正确的是( )
元素周期表是学习化学的重要工具,如图是元素周期表中的一格,以下对该图信息的解读中,不正确的是( )| A. | 该元素的原子序数为6 | |
| B. | 该元素所有原子的质子数均为6 | |
| C. | 该元素的原子质量为12.01 g | |
| D. | 该元素应有多种同位素,所有原子的中子数不都为6 |
7.下列各组物质,属于同分异构体的是( )
| A. | 正丁烷与异丁烷 | B. | 白磷和红磷 | ||
| C. | ${\;}_{1}^{1}$H2和${\;}_{1}^{2}$H2 | D. | H2O与H2O2 |
14.有一种有机物的键线式酷似牛形(如图所示),故称为牛式二烯炔醇(cowenyenynol).下列有关说法不正确的是( )

| A. | 该有机物的化学式为:C29H44O | |
| B. | 牛式二烯炔醇能使酸性高锰酸钾溶液褪色 | |
| C. | 1mol牛式二烯炔醇最多可与6molBr2发生加成反应 | |
| D. | 牛式二烯炔醇分子内能发生消去反应 |
11.下列化合物中,属于盐的是( )
| A. | H2O | B. | H2SO4 | C. | KOH | D. | KNO3 |
12.下列各组物质是同分异构体的是( )
| A. | 氯仿和三氯甲烷 | B. | 2,2-二甲基丁烷和新戊烷 | ||
| C. | 葡萄糖和果糖 | D. | 苯酚和苯甲醇 |