��Ŀ����
ij��Һ�п��ܺ�������6�������е�ij���֣�Cl-��SO42-��CO32-��NH4+��K����Na+��Ϊȷ����Һ��ɽ�������ʵ�飺
��ȡ200mL������Һ����������BaCl2��Һ����Ӧ�������ˡ�ϴ�ӡ�����ó���4.30g��������м�����������ᣬ��2.33g�������ܡ�
����ٵ���Һ�м���������NaOH��Һ�����ȣ������ܴ�ʹʪ���ɫʯ����ֽ����������1.12L(�ѻ���ɱ�״�����ٶ�����������ȫ���ݳ�)��
���ʴ��������⣺
(1)ԭ��Һ�У�c(CO32-)= mol/L��c(NH4+)= mol/L��
(2)ԭ��Һ�л�Ӧ�� ���Ӵ��ڣ������ʵ����ķ�Χ�� ��
��ϰ��ϵ�д�
�����Ŀ


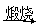 SO3
SO3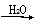 H2SO4
H2SO4 Na
Na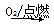 Na2O2
Na2O2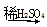 FeSO4(aq)
FeSO4(aq)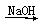 Fe(OH)2
Fe(OH)2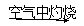 Fe2O
Fe2O 3
3 FeCl3(aq)
FeCl3(aq) 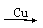 Fe
Fe ����������CO2�ͷ�O2�Ĺ��̿�������Ϊ����������
����������CO2�ͷ�O2�Ĺ��̿�������Ϊ����������
 1/2CH3OH(g) ��H=-45.4kJ��mol-1��
1/2CH3OH(g) ��H=-45.4kJ��mol-1��