题目内容
17.一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-,下列对该燃料电池的说法正确的是( )| A. | 电池的总反应是:2C4H10+13O2+16OH-═8CO32-+18H2O | |
| B. | 在熔融电解质中,O2-移向负极 | |
| C. | 通入空气一极是负极,电极反应为:O2+4e-═2O2- | |
| D. | 通入丁烷一极是正极,电极反应为:C4H10+13O2--26e-═4CO2+5H2O |
分析 所有燃烧电池中,通入燃料的电极是负极、通入氧化剂的电极是正极,所以该燃料电池中通入丁烷的电极是负极、通入空气的电极是正极,负极反应式为C4H10+13O2--26e-═4CO2+5H2O、正极反应式为O2+4e-═2O2-,则电池反应式为2C4H10+13O2═8CO2+10H2O,电解质中阴离子向负极移动、阳离子向正极移动,据此分析解答.
解答 解:A.该燃料电池中,负极反应式为C4H10+13O2--26e-═4CO2+5H2O、正极反应式为O2+4e-═2O2-,则电池反应式为2C4H10+13O2═8CO2+10H2O,故A错误;
B.放电时,电解质中阴离子向负极移动、阳离子向正极移动,所以O2-移向负极,故B正确;
C.通入空气的电极是正极,电极反应式为O2+4e-═2O2-,故C错误;
D.通入丁烷的电极是负极,电极反应为:C4H10+13O2--26e-═4CO2+5H2O,故D错误;
故选B.
点评 本题考查化学电源新型电池,为高频考点,明确各个电极上发生的反应是解本题关键,难点是电极反应式的书写,注意该电解质溶液不是酸或碱,为易错点.

练习册系列答案
相关题目
7.二氧化锰是制造锌锰干电池的基本材料.工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如图1:
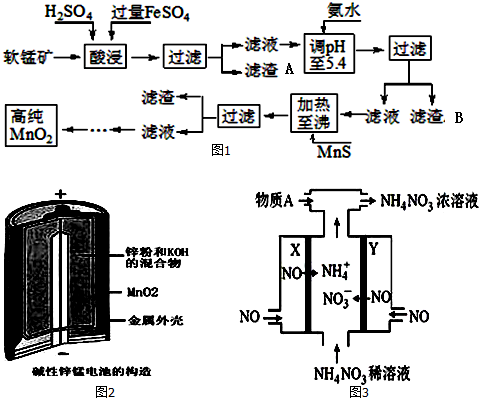
某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH如表,回答下列问题
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为MnO2+2FeSO4+2H2SO4═MnSO4+Fe2(SO4)3+2H2O.
(2)滤渣A的主要成分是SiO2;滤渣B的主要成分是Fe(OH)3、Al(OH)3.
(3)加入MnS的目的是除去Cu2+、Zn2+杂质.可能原因是CuS、ZnS的溶解度较MnS小.
(4)碱性锌锰电池是一种一次性电池,其结构如图2所示.该电池放电过程产生MnOOH.该电池的正极反应式为MnO2+H2O+e-═MnO(OH)+OH-,电池总反应的方程式为Zn+2MnO2+2H2O═2MnOOH+ZnOH)2.
(5)利用该碱性锌锰电池电解NO制备NH4NO3,其工作原理如图3所示,X电极阴极,电解时阳极的电极反应为NO-3e-+2H2O=NO3-+4H+,使电解产物全部转化为NH4NO3,需补充物质A,A是NH3.

某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH如表,回答下列问题
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 | CuS | ZnS | MnS | FeS |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 | ≥-0.42 | ≥2.5 | ≥7 | ≥7 |
(2)滤渣A的主要成分是SiO2;滤渣B的主要成分是Fe(OH)3、Al(OH)3.
(3)加入MnS的目的是除去Cu2+、Zn2+杂质.可能原因是CuS、ZnS的溶解度较MnS小.
(4)碱性锌锰电池是一种一次性电池,其结构如图2所示.该电池放电过程产生MnOOH.该电池的正极反应式为MnO2+H2O+e-═MnO(OH)+OH-,电池总反应的方程式为Zn+2MnO2+2H2O═2MnOOH+ZnOH)2.
(5)利用该碱性锌锰电池电解NO制备NH4NO3,其工作原理如图3所示,X电极阴极,电解时阳极的电极反应为NO-3e-+2H2O=NO3-+4H+,使电解产物全部转化为NH4NO3,需补充物质A,A是NH3.
8.关于化学平衡常数的叙述正确的是( )
| A. | 温度一定,一个化学反应的平衡常数是一个常数 | |
| B. | 两种物质反应,不管怎样书写化学方程式,平衡常数不变 | |
| C. | 温度一定时,对于给定的化学反应,正、逆反应的平衡常数互为倒数 | |
| D. | 浓度商Qc<Kc,v(正)<v(逆) |
5.一瓶Na2SO3已部分被氧化,必须通过实验确定其纯度,正确的操作顺序是( )
①称取样品;②用蒸馏水溶解样品;③过滤;④在烘箱中烘干沉淀;
⑤向溶液中加过量的用盐酸酸化的BaCl2溶液;⑥用蒸馏水洗涤沉淀并再用AgNO3溶液检验,不出现沉淀为止;⑦准确称量干燥沉淀的质量;⑧在干燥器中冷却;⑨计算.
①称取样品;②用蒸馏水溶解样品;③过滤;④在烘箱中烘干沉淀;
⑤向溶液中加过量的用盐酸酸化的BaCl2溶液;⑥用蒸馏水洗涤沉淀并再用AgNO3溶液检验,不出现沉淀为止;⑦准确称量干燥沉淀的质量;⑧在干燥器中冷却;⑨计算.
| A. | ①②③⑥⑤④⑧⑦⑨ | B. | ①②⑤③⑥④⑧⑦⑨ | C. | ①②③④⑤⑧⑥⑦⑨ | D. | ①②③⑤⑥④⑧⑦⑨ |
12.设NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,2.24LCH2Cl2含有分子的数目为0.1NA | |
| B. | 电解精炼铜时,阳极质量减少12.8g时,转移电子0.4NA | |
| C. | 25℃,pH=11的Na2CO3溶液中由水电离出的H+的数目为10-3NA | |
| D. | 常温常压下,将0.1mol Fe投入足量的稀硝酸中,转移的电子为0.3 NA |
2.利用如图所示装置进行相关实验能实现目标的是( )


| A. | 若I中装过量高锰酸钾溶液,Ⅱ中装澄清石灰水,则能检验SO2中是否混有CO2 | |
| B. | 若I中装足量澄清石灰水,Ⅱ中装浓硫酸,则能测定CO2和水蒸气的混合气体中水蒸气的含量 | |
| C. | 若I中装足量饱和碳酸钠溶液,Ⅱ中装浓硫酸,则能除去CO2中混有的HCl | |
| D. | 若I中装BaCl2溶液,Ⅱ中装水,则能证明SO2和NO2混合气体中SO2不与BaCl2反应 |
9.某工厂从废含镍有机催化剂中回收镍的工艺流程如图所示(已知废催化剂中舍有Ni70.0%及一定量的Al、Fe、SiO2和有机物,镍及其化台物的化学性质与铁的类似,但Ni2-的性质较稳定).
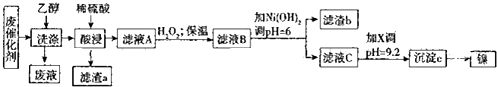
已知:部分阳离子以氢氧化物的形式完全沉淀时的pH如下表所示,回答下列间题
(1)滤渣a的成分是SiO2,用乙醇洗涤废催化剂的目的是溶解、除去有机物,从废渣中回收乙醇的方法是蒸馏.
(2)为提高酸浸速率,可采取的措施有(答两条)将废催化剂粉碎或适当地提高硫酸的浓度、浸泡时的温度.
(3)向A中加人 H2O2时反应的离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O.试剂x可以是蒸馏.
(4)用方程式表示出由沉淀.制取单质镍的方法Ni(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$NiO+H2O、2Al+2NiO $\frac{\underline{\;高温\;}}{\;}$Al2O3+3Ni.回收mkg上述废催化剂的过程中,若将溶液pH调整为6时消耗了akgNi(OH)2,从洗涤到得到滤液B的过程中镍的损失率为3%,后几步操作过程中镍的损失率为5%,则最终得到单质镍的质量为(70%×97%m+$\frac{59}{93}$a)×95%kg(填计算式).
(5)利用化学镀(待镀件直接置于含有镀层金属的化合物的溶液中)可以在金属、塑料、陶瓷等物品表面镀上一层金属镍或铬等金属,某化学镀镍的溶液中含有Ni2+和H2PO2-,在酸性条件下发生的反应之一如下,请配平该反应.与电镀相比,化掌镀的最大优点是:不消耗电能,节约能源.

已知:部分阳离子以氢氧化物的形式完全沉淀时的pH如下表所示,回答下列间题
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
(2)为提高酸浸速率,可采取的措施有(答两条)将废催化剂粉碎或适当地提高硫酸的浓度、浸泡时的温度.
(3)向A中加人 H2O2时反应的离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O.试剂x可以是蒸馏.
(4)用方程式表示出由沉淀.制取单质镍的方法Ni(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$NiO+H2O、2Al+2NiO $\frac{\underline{\;高温\;}}{\;}$Al2O3+3Ni.回收mkg上述废催化剂的过程中,若将溶液pH调整为6时消耗了akgNi(OH)2,从洗涤到得到滤液B的过程中镍的损失率为3%,后几步操作过程中镍的损失率为5%,则最终得到单质镍的质量为(70%×97%m+$\frac{59}{93}$a)×95%kg(填计算式).
(5)利用化学镀(待镀件直接置于含有镀层金属的化合物的溶液中)可以在金属、塑料、陶瓷等物品表面镀上一层金属镍或铬等金属,某化学镀镍的溶液中含有Ni2+和H2PO2-,在酸性条件下发生的反应之一如下,请配平该反应.与电镀相比,化掌镀的最大优点是:不消耗电能,节约能源.
6. 苯甲酸钠是一种常见的食品防腐剂.实验室制备苯甲酸的反应装置图和有关数据如下:
苯甲酸钠是一种常见的食品防腐剂.实验室制备苯甲酸的反应装置图和有关数据如下:
按下列合成步骤回答问题:
(1)制备苯甲酸
在三颈瓶中加入4mL甲苯和20mL稀硫酸,放入碎瓷片后,加热至沸腾,加入12.8g高锰酸钾,加热到甲苯层消失.将三颈瓶在冰水浴中冷却,分离出苯甲酸.
①球形冷凝管的作用是冷凝回流,其进水口是b(填“a”或“b”).
②三颈瓶中反应的离子方程式 .
.
③分离苯甲酸选用的玻璃仪器是BCD(填标号)
A分液漏斗 B玻璃棒 C烧杯 D漏斗 E蒸馏烧瓶 F直形冷凝管
④分离出的苯甲酸晶体中可能含有的杂质是K2SO4、MnSO4,为进一步提纯,应采用的方法是重结晶.
(2)制备苯甲酸钠
控制温度为70℃,向三颈瓶中加入61.0g苯甲酸和适量的32%的碳酸钠溶液,充分反应后停止加热.在深色的溶液中加入活性炭,并将反应混合物过滤,得到无色透明的苯甲酸钠溶液,将滤液转入蒸发皿中,加热蒸发、冷却结晶,过滤、洗涤、干燥制得苯甲酸钠晶体.
⑤控制温度为70℃的方法是水浴加热.
⑥加入活性炭的作用是吸附色素.
⑦若提纯得到46.8g苯甲酸钠.则苯甲酸钠的产率是65.0%.
 苯甲酸钠是一种常见的食品防腐剂.实验室制备苯甲酸的反应装置图和有关数据如下:
苯甲酸钠是一种常见的食品防腐剂.实验室制备苯甲酸的反应装置图和有关数据如下:| 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | |
| 甲苯 | 92 | -94.9 | 110.6 | 难溶于水 |
| 苯甲酸 | 122 | 122.13 | 249 | 微溶于水 |
| 苯甲酸钠 | 144 | - | 249.3 | 易溶于水 |
(1)制备苯甲酸
在三颈瓶中加入4mL甲苯和20mL稀硫酸,放入碎瓷片后,加热至沸腾,加入12.8g高锰酸钾,加热到甲苯层消失.将三颈瓶在冰水浴中冷却,分离出苯甲酸.
①球形冷凝管的作用是冷凝回流,其进水口是b(填“a”或“b”).
②三颈瓶中反应的离子方程式
 .
.③分离苯甲酸选用的玻璃仪器是BCD(填标号)
A分液漏斗 B玻璃棒 C烧杯 D漏斗 E蒸馏烧瓶 F直形冷凝管
④分离出的苯甲酸晶体中可能含有的杂质是K2SO4、MnSO4,为进一步提纯,应采用的方法是重结晶.
(2)制备苯甲酸钠
控制温度为70℃,向三颈瓶中加入61.0g苯甲酸和适量的32%的碳酸钠溶液,充分反应后停止加热.在深色的溶液中加入活性炭,并将反应混合物过滤,得到无色透明的苯甲酸钠溶液,将滤液转入蒸发皿中,加热蒸发、冷却结晶,过滤、洗涤、干燥制得苯甲酸钠晶体.
⑤控制温度为70℃的方法是水浴加热.
⑥加入活性炭的作用是吸附色素.
⑦若提纯得到46.8g苯甲酸钠.则苯甲酸钠的产率是65.0%.
7.向下列溶液中分别加入钠的小颗粒,溶液里无固体析出的是( )
| A. | BaCl2溶液 | B. | NaOH饱和溶液 | C. | CuSO4溶液 | D. | 盐酸 |