题目内容
现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子Li+、K+、Cu2+、Ba2+、Al3+和五种阴离子X、Cl-、OH-、NO3-、CO32-中的一种.已知E是LiCl.
(1)写出LiCl电子式 .如果在LiCl溶液中加入NaF的反应为:Li++F-?LiF↓,该反应的平衡常数表达式为K= .
(2)某同学通过比较分析,认为无须检验就可判断其余的四种物质中必有的两种物质是 和 (填对应物质的化学式).
(3)物质C中含有离子X.为了确定X,现将(2)中的两种物质记为A和B,当C与A的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固体.则X为 (填序号).
①Br- ②SO42- ③CH3COO- ④HCO3-
(4)已知B物质A2B型,属于反萤石(CaF2)结构,其阴离子做面心立方最密堆积,则阳离子旁最近的阳离子配位数是 .
(5)将19.2g Cu投入装有足量D溶液的试管中,Cu不溶解,再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,写出Cu溶解的离子方程式 ,若要Cu完全溶解,至少加入H2SO4的物质的量是 mol.
(1)写出LiCl电子式
(2)某同学通过比较分析,认为无须检验就可判断其余的四种物质中必有的两种物质是
(3)物质C中含有离子X.为了确定X,现将(2)中的两种物质记为A和B,当C与A的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固体.则X为
①Br- ②SO42- ③CH3COO- ④HCO3-
(4)已知B物质A2B型,属于反萤石(CaF2)结构,其阴离子做面心立方最密堆积,则阳离子旁最近的阳离子配位数是
(5)将19.2g Cu投入装有足量D溶液的试管中,Cu不溶解,再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,写出Cu溶解的离子方程式
考点:无机物的推断,晶胞的计算,离子共存问题
专题:离子反应专题,化学键与晶体结构
分析:CO32-与Cu2+、Ba2+、Al3+不能大量共存,OH-与Al3+、Cu2+不能大量共存,E为LiCl,则必有的两种物质记为A、B,A、B分别为K2CO3、Ba(OH)2,C与A的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固体,蓝色沉淀为氢氧化铜,白色沉淀为硫酸钡,则A应为Ba(OH)2,C中含SO42-,则C为CuSO4,D为Al(NO3)3,以此解答该题.
解答:
解:CO32-与Cu2+、Ba2+、Al3+不能大量共存,OH-与Al3+、Cu2+不能大量共存,E为LiCl,则必有的两种物质记为A、B,A、B分别为K2CO3、Ba(OH)2,C与A的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固体,蓝色沉淀为氢氧化铜,白色沉淀为硫酸钡,则A应为Ba(OH)2,C中含SO42-,则C为CuSO4,D为Al(NO3)3,
(1)LiCl电子式为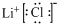 ,Li++F-?LiF↓,该反应的平衡常数表达式为K=
,Li++F-?LiF↓,该反应的平衡常数表达式为K=
,故答案为: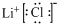 ;
;
;
(2)由上述分析可知,必有的两种物质为K2CO3、Ba(OH)2,故答案为:K2CO3;Ba(OH)2;
(3)由上述分析可知,C为CuSO4,C中X为SO42-,故答案为:②;
(4) CaF2晶胞中每个Ca2+连接8个氟离子,每个氟离子连4个钙离子,B为K2CO3,反萤石(CaF2)结构,其阴离子做面心立方最密堆积,
CaF2晶胞中每个Ca2+连接8个氟离子,每个氟离子连4个钙离子,B为K2CO3,反萤石(CaF2)结构,其阴离子做面心立方最密堆积,
K+位于体心,8个K+形成正立方体,阳离子最近的K+位于顶点,即边长的距离最近,则配位数是6,
故答案为:6;
(5)根据以上推断可知D中含有NO3-,已知将19.2gCu投入装有足量D溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,
发生的反应为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O
则n(Cu)=mM=
=0.3mol,
有方程可知
=
,
所以n(H+)=0.8mol,
所以n(H2SO4)=12n(H+)=0.4mol,
故答案为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;0.4mol.
(1)LiCl电子式为
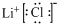 ,Li++F-?LiF↓,该反应的平衡常数表达式为K=
,Li++F-?LiF↓,该反应的平衡常数表达式为K=| 1 |
| [c(Li+)?c(F-)] |
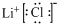 ;
;| 1 |
| [c(Li+)?c(F-)] |
(2)由上述分析可知,必有的两种物质为K2CO3、Ba(OH)2,故答案为:K2CO3;Ba(OH)2;
(3)由上述分析可知,C为CuSO4,C中X为SO42-,故答案为:②;
(4)
 CaF2晶胞中每个Ca2+连接8个氟离子,每个氟离子连4个钙离子,B为K2CO3,反萤石(CaF2)结构,其阴离子做面心立方最密堆积,
CaF2晶胞中每个Ca2+连接8个氟离子,每个氟离子连4个钙离子,B为K2CO3,反萤石(CaF2)结构,其阴离子做面心立方最密堆积,K+位于体心,8个K+形成正立方体,阳离子最近的K+位于顶点,即边长的距离最近,则配位数是6,
故答案为:6;
(5)根据以上推断可知D中含有NO3-,已知将19.2gCu投入装有足量D溶液的试管中,Cu不溶解;再滴加稀H2SO4,Cu逐渐溶解,
发生的反应为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O
则n(Cu)=mM=
| 19.2g |
| 64g/mol |
有方程可知
| 3 |
| 8 |
| 0.3mol |
| n(H+) |
所以n(H+)=0.8mol,
所以n(H2SO4)=12n(H+)=0.4mol,
故答案为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;0.4mol.
点评:本题考查无机物的推断,为高频考点,物质推断为解答的关键,涉及离子检验、氧化还原反应及晶体分析等,题目难度较大,综合度较高,旨在考查学生的推断能力与方案设计能力,注意根据反应现象进行推断.

练习册系列答案
相关题目
若NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、7.8g Na2O2所含离子总数为0.4 NA |
| B、2.0gD2O(重水)含有的质子数是NA |
| C、标准状况下,0.5 NA个SO3分子所占的体积约为11.2 L |
| D、4℃时,18mL水分子中所含共价键的数目为4 NA |
下列物质属于电解质且能导电的是( )
| A、盐酸 |
| B、NaCl晶体 |
| C、熔融的NaCl |
| D、液态HCl |