题目内容
9.有两种金属的合金13 g,与足量稀硫酸反应后,在标准状况下产生气体11.2 L,则组成该合金的金属不可能是( )| A. | Mg和Al | B. | Mg和Zn | C. | Al和Zn | D. | Al和Fe |
分析 根据电子转移守恒计算出选项中各金属与稀硫酸反应产生11.2 L H2所需金属质量,13g介于两种金属质量之间,若金属不与硫酸反应生成氢气,其质量视作无穷大.
解答 解:标况下11.2L 氢气物质的量为$\frac{11.2L}{22.4L/mol}$=0.5mol,则转移电子为0.5mol×2=1mol,
需要Mg的质量为$\frac{1mol}{2}$×24g/mol=12g,
需要Al的质量为$\frac{1mol}{3}$×27g/mol=9g,
需要Zn的质量$\frac{1mol}{2}$×65g/mol=32.5g,
需要Fe的质量$\frac{1mol}{2}$×56g/mol=28g,
13g介于两质量之间的组合不可能是Al和Mg,
故选:A.
点评 本题考查混合物计算、金属与酸的反应,题目利用极限法进行分析解答,侧重考查学生分析计算能力.

练习册系列答案
相关题目
20.NA为阿伏加德罗常数,下列叙述正确的是( )
| A. | 22.4LCH4和CH3Cl的混合物所含有的分子数目为NA | |
| B. | 1mol过氧化氢分子中共用电子对数为3NA | |
| C. | 用惰性电极电解1 L浓度均为2 mol/L的AgNO3与Cu(NO3)2的混合溶液,当有0.2 NA个电子转移时,阴极析出6.4g金属 | |
| D. | 0.1mol Na2CO3•10H2O在晶体中或溶液中,含有的CO32-离子均小于0.1 NA |
17.在复杂的体系中,确认化学反应先后顺序有利于解决问题.下列化学反应先后顺序判断正确的是( )
| A. | 在含等物质的量的AlO2-、OH-、SO32-的溶液中,逐滴加入盐酸:AlO2-、OH-、SO32- | |
| B. | 在含等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气:I-、Br-、Fe2+ | |
| C. | 在含等物质的量的Ba(OH)2、KOH的溶液中缓慢通入SO2:KOH、Ba(OH)2、BaSO3 | |
| D. | 在含等物质的量的Fe2+、Ag+、Cu2+、H+的溶液中加入锌粉:Ag+、Cu2+、H+、Fe2+ |
14.将下列各组溶液混合,不能发生复分解反应的是( )
| A. | NaOH溶液、稀盐酸 | B. | NaCl溶液、KNO3溶液 | ||
| C. | Na2CO3溶液、澄清石灰水 | D. | Na2CO3溶液、稀硝酸 |
1.铅蓄电池的工作原理为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,下列判断正确的是( )


| A. | K闭合时,c电极反应式:PbSO4+2H2O-2e-=PbO2+4H++SO42- | |
| B. | 当电路中转移0.4mol电子时,I中消耗的H2SO4为0.2 mol | |
| C. | K闭合时,II中SO42-向c电极迁移 | |
| D. | K闭合一段时间后,II可单独作为电源,d电极为正极 |
10.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 0.1 mol•L-1的BaCl2溶液中:K+、Na+、OH-、NO3- | |
| B. | 使甲基橙变红的溶液中:Ca2+、NH4+、CH3COO-、Cl- | |
| C. | 无色透明的溶液中:Fe2+、SO42-、NO3-、Na+ | |
| D. | 由水电离出的c(H+)=10-12 mol•L-1的溶液中:Mg2+、K+、Br-、HCO3- |
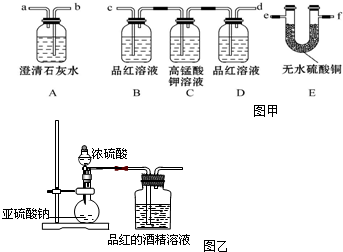
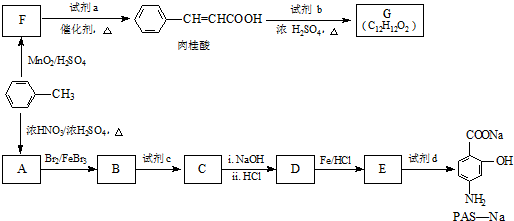
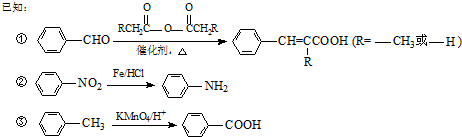
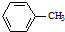 生成A的反应类型是取代反应.
生成A的反应类型是取代反应.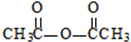 .
.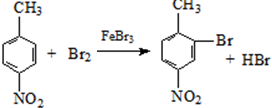 .
.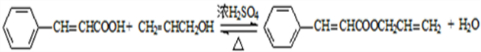 .
. .
.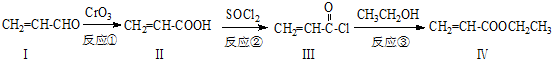
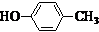 也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为
也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为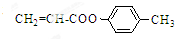 .
.