题目内容
1.在证明海带中存在碘元素的实验操作中,主要仪器选用错误的是( )| 选项 | 操作 | 主要仪器 |
| A | 称取3.0g干海带 | 托盘天平 |
| B | 灼烧干海带至完全变成灰烬 | 烧杯 |
| C | 过滤煮沸后的海带灰与水的混合液 | 漏斗 |
| D | 用四氯化碳从氧化后的海带灰浸取液中提取碘 | 分液漏斗 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.可用托盘天平称量药品的质量;
B.灼烧固体药品,应在坩埚中进行;
C.过滤的主要仪器为漏斗;
D.碘易溶于四氯化碳.
解答 解:A.可用托盘天平称取3.0g干海带,故A正确;
B.灼烧固体药品,所用仪器应耐高温,应在坩埚中进行,故B错误;
C.过滤的主要仪器为漏斗,故C正确;
D.碘易溶于四氯化碳,可用分液漏斗,用萃取的方法分离,故D正确.
故选B.
点评 本题考查海水提碘及实验评价,为高频考点,把握提纯碘单质的实验流程及发生的反应、混合物分离方法为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案
相关题目
9. 氢氧燃料电池是一种能在航天飞机上使用的特殊电池,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池是一种能在航天飞机上使用的特殊电池,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
 氢氧燃料电池是一种能在航天飞机上使用的特殊电池,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池是一种能在航天飞机上使用的特殊电池,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )| A. | A电极是负极,电极上发生氧化反应 | |
| B. | 该电池总反应:2H2+O2═2H2O | |
| C. | 由于A、B两电极没有活动性差别,不能构成原电池 | |
| D. | 外电路中电流由B电极通过导线流向A电极 |
16.在元素周期表中金属与非金属的分界处,可以找到( )
| A. | 合金 | B. | 农药 | C. | 催化剂 | D. | 半导体材料 |
6.阿托酸是一种常用的医药中间体,其结构如图所示.下列关于阿托酸的说法正确的是( )

| A. | 分子式为C9H10O2 | |
| B. | 能发生取代、加聚、氧化等反应 | |
| C. | 不能与Na2CO3溶液反应放出气体 | |
| D. | 1 mol阿托酸最多能和5 mol Br2发生加成反应 |
6.下列表达正确的是( )
| A. | N2的电子式为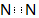 | B. | H2S的电子式可表示为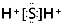 | ||
| C. | 用电子式表示Na2O的形成过程为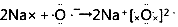 | D. | MgCl2的电子式为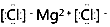 |
3.已知:①能量越低的物质就越稳定,②白磷转化成红磷是放热反应.据此,下列判断或说法中正确的是( )
| A. | 在相同的条件下,白磷比红磷稳定 | |
| B. | 在相同的条件下,红磷比白磷稳定 | |
| C. | 在相同的条件下,红磷所具有的总能量比白磷高 | |
| D. | 在相同的条件下,相同质量的红磷和白磷完全燃烧放出的热量相等 |
4.已知反应:2NO2(红棕色)?N2O4(无色),分别进行如下两个实验:
实验ⅰ:将NO2球分别浸泡在热水和冰水中,现象如图1.
实验ⅱ:将一定量的NO2充入注射器中后封口,测定改变注射器体积的过程中气体透光率随时间的变化(气体颜色越深,透光率越小),如图2.下列说法不正确的是( )

实验ⅰ:将NO2球分别浸泡在热水和冰水中,现象如图1.
实验ⅱ:将一定量的NO2充入注射器中后封口,测定改变注射器体积的过程中气体透光率随时间的变化(气体颜色越深,透光率越小),如图2.下列说法不正确的是( )

| A. | 图1现象说明该反应为放热反应 | |
| B. | 图2中b点的操作是压缩注射器体积 | |
| C. | c点:v (正)<v (逆) | |
| D. | 若不忽略体系温度变化,且没有能量损失,则T(d)>T(c) |
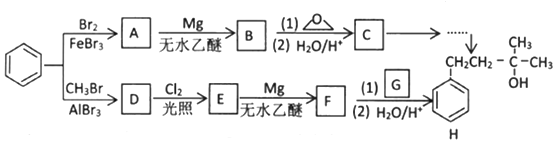
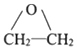 →R-CH2CH2OMgX<“m“:math dsi:zoomscale=150 dsi:_mathzoomed=1>→H2O/H+$\stackrel{H_{2}O/H+}{→}$R-CH2CH2OH
→R-CH2CH2OMgX<“m“:math dsi:zoomscale=150 dsi:_mathzoomed=1>→H2O/H+$\stackrel{H_{2}O/H+}{→}$R-CH2CH2OH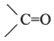 →
→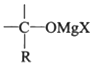 $\stackrel{H_{2}O/H+}{→}$
$\stackrel{H_{2}O/H+}{→}$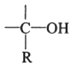
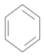 +CH3Br$→_{.}^{AlBr_{3}}$
+CH3Br$→_{.}^{AlBr_{3}}$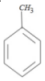 +HBr
+HBr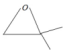
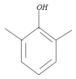 ,
,