题目内容
下列关于氢氧化钠与醋酸两种稀溶液的说法正确的是( )
| A、相同浓度的两溶液中由水电离出的c(H+)相同 |
| B、pH=12与pH=2的两溶液稀释100倍,pH都变化2个单位 |
| C、用20mL0.1mol/L的氢氧化钠滴定未知浓度的醋酸,选用酚酞作指示剂 |
| D、两溶液相互反应生成1molH2O的中和热为57.3kJ/mol |
考点:弱电解质在水溶液中的电离平衡,pH的简单计算
专题:电离平衡与溶液的pH专题
分析:A、醋酸是弱酸,不能完全电离;
B、醋酸是弱酸,稀释时会有醋酸继续电离,氢离子物质的量增大;
C、用碱滴定酸时,选用无色的酚酞作指示剂,溶液颜色变化明显;
D、醋酸是弱酸没有完全电离,其电离吸热.
B、醋酸是弱酸,稀释时会有醋酸继续电离,氢离子物质的量增大;
C、用碱滴定酸时,选用无色的酚酞作指示剂,溶液颜色变化明显;
D、醋酸是弱酸没有完全电离,其电离吸热.
解答:
解:A醋酸电离出来的氢离子浓度比氢氧化钠电离出来的氢氧根离子浓度小,对水电离的抑制能力差,故A错误;
B、弱电解质pH变化小,醋酸pH变化小于2,故B错误;
C、用碱滴定酸时,选用无色的酚酞作指示剂,溶液颜色变化明显,故C正确;
D、两溶液相互反应生成1molH2O的中和热小于57.3kJ/mol,故D错误;
故选C.
B、弱电解质pH变化小,醋酸pH变化小于2,故B错误;
C、用碱滴定酸时,选用无色的酚酞作指示剂,溶液颜色变化明显,故C正确;
D、两溶液相互反应生成1molH2O的中和热小于57.3kJ/mol,故D错误;
故选C.
点评:本题考查了弱电解质的不完全电离,存在电离平衡,注意其电离是吸热的,题目难度不大.

练习册系列答案
相关题目
下列物质中,能用来检验酒精中是否含有水的是( )
| A、生石灰 | B、浓硫酸 |
| C、无水硫酸铜 | D、金属钠 |
下列有关蛋白质的叙述中,不正确的是( )
| A、蛋白质溶液中加入饱和(NH4)2SO4溶液,蛋白质析出,再加水也不溶解 |
| B、人工合成的具有生命活性的蛋白质-结晶牛胰岛素是1965年我国科学家最先合成的 |
| C、重金属盐能使蛋白质变性,所以误食重金属盐会中毒 |
| D、浓HNO3溅在皮肤上,使皮肤呈黄色,是由于浓HNO3和蛋白质发生颜色反应 |
下列关于实验现象的描述不正确的是( )
| A、把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| B、用锌片做阳极,铁片做阴极,电解氯化铜溶液,铁片表面析出铜 |
| C、把铜片插入三氯化铁溶液,在铜片表面析出铁 |
| D、把锌放入稀盐酸中,加几滴氯化铜溶液,产生气泡速率加快 |
水是人类赖以生存的重要物质,水污染却严重影响着人类的生存环境.目前,水污染主要来自 ( )
①工业生产中废渣、废液的任意排放
②农业生产中农药、化肥的过量使用
③城市生活污水的任意排放
④生活垃圾和废旧电池的随意丢弃.
①工业生产中废渣、废液的任意排放
②农业生产中农药、化肥的过量使用
③城市生活污水的任意排放
④生活垃圾和废旧电池的随意丢弃.
| A、①② | B、②③④ |
| C、①③④ | D、①②③④ |
X、Y、Z、R为前四周期元素且原子序数依次增大.X的单质与氢气可以化合生成气体G,其水溶液pH>7;Y单质是一种黄色固体;R是一种应用最广的金属,它的一种含氧酸根化学式为RO42-,且具有强氧化性,在其钠盐中加入稀硫酸,溶液变为黄色,并有无色气体产生.Y、Z分别与钠元素可以形成化合物Q和J,J的水溶液与AgNO3溶液反应可生成不溶于稀硝酸的白色沉淀L;Z与氢元素形成的化合物与G反应生成M.则下列说法不正确的是( )
| A、M是离子化合物,且其溶液中阴阳离子个数比为1:1 |
| B、L的悬浊液加入Q的溶液,白色沉淀可以转化为黑色沉淀 |
| C、Na2RO4水溶液可以用于杀菌消毒和净水 |
| D、Q的水溶液中加入铝与Z单质形成的化合物,只有白色沉淀生成 |
下列化学方程式改写成离子方程式不正确的是( )
| A、CuCl2+2NaOH═Cu(OH)2↓+2NaCl;Cu2++20H═Cu(OH)2↓ |
| B、BaSO4+2HCl═BaCl2+CO2↑+H2O;SO42-+2H+═CO2↑+H2O |
| C、Ca(NO3)2+Na2CO3═CaCO3↓+2NaNO3 Ca2++CO32-═CaCO3↓ |
| D、2KOH+H2SO4═K2SO4+2H2O;H++OH-═H2O |
已知链式炔碳C300经过适当处理可得含多个 (不含
(不含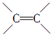 )的链状化合物C300H298,则该分子中含
)的链状化合物C300H298,则该分子中含 的个数为( )
的个数为( )
 (不含
(不含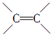 )的链状化合物C300H298,则该分子中含
)的链状化合物C300H298,则该分子中含 的个数为( )
的个数为( )| A、70 | B、72 | C、74 | D、76 |
染料敏化太阳能电池(简称DSC)工作时类似叶绿素的染料吸收太阳光,产生电子,电子再被电极收集,然后通过外电路,回到反电极产生光电流.该过程中的能量转化形式为( )
| A、太阳能→电能 |
| B、太阳能→化学能 |
| C、化学能→电能 |
| D、电能→化学能 |