题目内容
已知:2H2(g) +O2(g) =2H2O( l ) 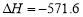 kJ·mol-1
kJ·mol-1
CH4(g) +2O2(g) =CO2(g) +2H2O( l ) 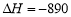 kJ·mol-1
kJ·mol-1
现有H2与CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2和H2O( l ),若实验测得反应放热3695 kJ,则原混合气体中H2与CH4的物质的量之比是
A.1:1 B.1:3 C.1:4 D.2:3
B
【解析】
试题分析:根据题意,H2的燃烧热方程式为:H2(g) +1/2O2(g) =H2O( l ) △H=-285.8 kJ·mol-1,设H2与CH4的物质的量分别为:xmol和ymol,可列出方程式:x+y=112/22.4=5 285.8x +890y=3695 得:x=1.25mol,y=3.75mol,故H2与CH4的物质的量之比是1:3
考点:反应热的有关计算。

练习册系列答案
相关题目
将NaOH溶液与CuSO4溶液加入某病人的尿液中,微热时如果观察到红色沉淀,则说明该病人的尿液中含有
| A.乙酸 | B.乙醇 | C.氯化钠 | D.葡萄糖 |
 B.CF2=CF2 C.CH≡C—CH=CH2 D.CO2
B.CF2=CF2 C.CH≡C—CH=CH2 D.CO2 2C,在反应过程中C的物质的量分数随温度变化
2C,在反应过程中C的物质的量分数随温度变化
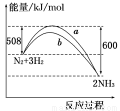
 2NH3 ΔH=-92 kJ/mol
2NH3 ΔH=-92 kJ/mol 2AB2(g)的ΔH<0,下列说法正确的是
2AB2(g)的ΔH<0,下列说法正确的是