题目内容
实验室里有4个药品橱,已经存放以下列试剂:
药品橱 | 甲橱 | 乙橱 | 丙橱 | 丁橱 |
药品 | 醋酸,乙醇 | CuSO4·5H2O,MgCl2 | 白磷,硫黄 | 镁条,锌粒 |
实验室新购 进一些碘化钾,应该将这些碘化钾放在
进一些碘化钾,应该将这些碘化钾放在
A.甲橱 B.乙橱 C.丙橱 D.丁橱
完成下列问题:
I.(1)某学习小组用0.80 mol/L标准浓度的氢氧化钠溶液测定未知浓度的盐酸。
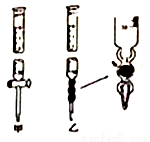
①滴定管如图所示,用 (填“甲”或“乙”)滴定管盛待测定的未知浓度的盐酸溶液。
②用滴定的方法来测定盐酸的浓度,实验数据如下所示:
实验编号 | 待测盐酸溶液的体积/mL | 滴入NaOH溶液的体积/mL |
1 | 20.00 | 23.00 |
2 | 20.00 | 23.10 |
3 | 20.00 | 22.90 |
该未知盐酸的浓度为_______________(保留两位有效数字)。
(2)若用酚酞作指示剂,达到滴定终点的标志是____________________。
(3)造成测定结果偏高的操作可能是__________。
A.盛装待测液的锥形瓶用水洗后未干燥
B.滴定前,碱式滴定管尖端有气泡,滴定后气泡消失
C.碱式滴定管用蒸馏水洗净后,未用标准氢氧化钠溶液润洗
D.读碱式滴定管的读数时,滴定前仰视凹液面最低处,滴定后俯视读数
II.为了测定某氯化锶(SrCl2)样品的纯度,探究活动小组设计了如下方案:
①称取1.0 g样品溶解于适量水中,向其中加入含AgNO3 2.38 g的AgNO3溶液(溶液中除Cl-外,不含其他与Ag+反应生成沉淀的离子),Cl-即被全部沉淀。
②用含Fe3+的溶液作指示剂,用0.2 mol·L-1的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出,以测定氯化锶样品的纯度。
请回答下列问题:
(1)用含Fe3+的溶液作指示剂达到滴定终点时发生颜色变化的离子方程式:_____________。
(2)在终点到达之前的滴定过程中,两种沉淀表面会吸附部分Ag+,需不断剧烈摇动锥形瓶,否则会使n(Cl-)的测定结果________(选填“偏高”、“偏低”或“无影响”)。


 碳酸钠: ;
碳酸钠: ;
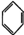 中含有的碳碳双键数为0.3NA
中含有的碳碳双键数为0.3NA 物质的食品
物质的食品 2PCl3(g)+Cl2(g)②2HI(g)
2PCl3(g)+Cl2(g)②2HI(g)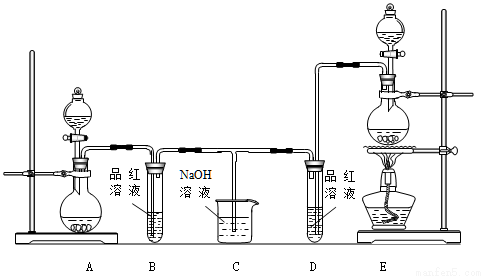
 MnCl2 + 2H2O + Cl2↑,应选用上图A、E装置中的 (填序号)制Cl2,反应中浓盐酸所表现出的性质是 、 。
MnCl2 + 2H2O + Cl2↑,应选用上图A、E装置中的 (填序号)制Cl2,反应中浓盐酸所表现出的性质是 、 。