题目内容
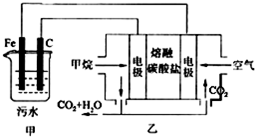 工业上常用Fe做电极电解处理含Cr2O72-的酸性废水,最终使铬元素以Cr(OH)3沉淀的形式除去.某科研小组用该原理处理污水,设计装置如图所示.下列说法不正确的是( )
工业上常用Fe做电极电解处理含Cr2O72-的酸性废水,最终使铬元素以Cr(OH)3沉淀的形式除去.某科研小组用该原理处理污水,设计装置如图所示.下列说法不正确的是( )| A、实验时若污水中离子浓度较小,导电能力较差,可加入适量的NaOH |
| B、燃料电池中若有1.6g CH4参加反应,则甲中C电极理论上生成气体体积为8.96L(标准状况下) |
| C、该燃料电池中阴离子移向甲烷一极 |
| D、甲中阳极附近溶液中的离子反应方程式是:Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.酸性废水中,加适量NaOH会与Fe2+反应生成Fe(OH)2;
B.甲中C电极发生2H2O=H2↑+2OH-,利用CH4~8e-~4H2↑来计算;
C.原电池中阴离子向负极移动;
D.亚铁离子具有还原性,Cr2O72-具有氧化性,发生氧化还原反应.
B.甲中C电极发生2H2O=H2↑+2OH-,利用CH4~8e-~4H2↑来计算;
C.原电池中阴离子向负极移动;
D.亚铁离子具有还原性,Cr2O72-具有氧化性,发生氧化还原反应.
解答:
解:A.酸性废水中,加适量NaOH会与阳极上电解生成的Fe2+反应生成Fe(OH)2,Fe2+被消耗,不能把溶液中Cr2O72-还原为Cr3+,故A错误;
B.甲中C电极发生2H2O=H2↑+2OH-,由CH4~8e-~4H2↑可知,1.6gCH4参加反应,则甲中C电极理论上生成气体体积为
×4×22.4L/mol=8.96L,故B正确;
C.原电池中阴离子向负极移动,即该燃料电池中阴离子移向甲烷一极,故C正确;
D.铁作阳极失电子得到的亚铁离子,亚铁离子会和Cr2O72-的酸性废水反应,发生反应的离子方程式是Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O,故D正确;
故选A.
B.甲中C电极发生2H2O=H2↑+2OH-,由CH4~8e-~4H2↑可知,1.6gCH4参加反应,则甲中C电极理论上生成气体体积为
| 1.6g |
| 16g/mol |
C.原电池中阴离子向负极移动,即该燃料电池中阴离子移向甲烷一极,故C正确;
D.铁作阳极失电子得到的亚铁离子,亚铁离子会和Cr2O72-的酸性废水反应,发生反应的离子方程式是Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O,故D正确;
故选A.
点评:本题考查了原电池、电解池及氧化还原反应,明确发生的电极反应是解答本题的关键,注重学生获取信息和应用信息的能力,题目难度中等.

练习册系列答案
相关题目
下列实验操作正确且能达到目的是( )
| A、结晶时,若溶质的溶解度越大,或溶液的浓度越高、或溶剂的蒸发速度越快,析出的晶粒就越细大 |
| B、用移液管量取液体,吸取液体后,将移液管垂直放入容器中,管尖与容器内壁不得接触,松开食指使溶液全部流出 |
| C、在温水瓶中加入Na2CO3溶液泡浸后加入盐酸能除去内壁CaSO4 |
| D、在两支试管中分别加1mL无水乙醇和1.5g苯酚固体,再加等量等体积的钠,比较乙醇、苯酚羟基上氢原子的活泼性 |
糖类、油脂和蛋白质的共同特点是( )
| A、均是高分子化合物 |
| B、常温下,遇碘水均会显蓝色 |
| C、均只含有C、H、O三种元素 |
| D、均是生命活动必不可少的物质 |
下列关于有机化合物的叙述错误的是( )
| A、甲烷和乙烯可以用溴水鉴别 |
| B、煤油是石油的分馏产品,可用于保存少量的钠 |
| C、棉花、蛋白质和油脂都是高分子化合物,水解产物均为电解质 |
| D、用饱和碳酸钠溶液可除去乙酸乙酯中混有的乙酸和乙醇 |
下列各离子浓度的大小比较,正确的是( )
| A、0.2 mol?L-1 Na2CO3溶液中:c (OH-)=c (HCO3-)+c (H+)+c (H2CO3) |
| B、常温时,将等体积的盐酸和氨水混合后,pH=7,则c (NH4+)>c (Cl-) |
| C、同浓度下列溶液中:①(NH4)2SO4 ②NH4HCO3 ③NH4Cl ④NH3?H2O,c(NH4+)由大到小的顺序是:①>③>②>④ |
| D、含有NH4+、Cl-、OH-、H+的溶液中,离子浓度一定是c (Cl-)>c (NH4+)>c (H+)>c (OH-) |
已知某一微粒的核电荷数,则下列一定可以确定的是其( )
| A、质子数 | B、核外电子数 |
| C、电子层数 | D、最外层电子数 |
X、Y、Z、R、W是原子序数依次增大的五种短周期元素.Y和R同主族,可组成共价化合物RY2和RY3,Y和Z最外层电子数之和与W的最外层电子数相同,25℃时0.01mol?L-1 X和W形成化合物的水溶液pH为2,下列说法正确的是( )
| A、非金属性Y>R,则Y的最高价氧化物水化物的酸性高于R的最高价氧化物水化物的酸性 |
| B、在Z、Y形成的两种离子化合物中阴阳离子的个数比分别为1:2和1:1 |
| C、原子半径由大到小排列的是:Z>R>W>Y>X |
| D、Y、Z、W三种元素组成化合物的水溶液一定显碱性 |
下列气体有颜色的是( )
| A、O2 |
| B、Cl2 |
| C、NH3 |
| D、NO |
短周期元素X、Y、Z的原子序数依次增大,Y为IA族元素,X与Z同主族,三种元素原子的最外层电子数之和为13.下列判断正确的是( )
| A、元素X位于第2周期第ⅣA族 |
| B、元素X分别与Y、Z形成的化合物都不止一种 |
| C、单核离子半径大小顺序:X>Y>Z |
| D、Z的最简单氢化物的稳定性比X的强 |