题目内容
4.用20克的烧碱配制成250mL的苛性钠溶液,其溶质的物质的量浓度为2mol/L;从中取出1mL,其物质的量浓度为2mol/L;含溶质的质量为0.08g;若将1mL的溶液加水稀释到100mL,所得溶液中溶质的物质的量浓度为0.02mol/L;其中含有钠离子的质量为0.046g.分析 根据n=cV,N=nNA计算;根据n=$\frac{m}{M}$,c=$\frac{n}{V}$计算;溶液为均一稳定分散系,取出任意体积都和原溶液浓度相等;根据溶液稀释前后溶质的物质的量不变计算稀释后溶质的物质的量浓度.
解答 解:n=$\frac{m}{M}$=$\frac{20g}{40g/mol}$=0.5mol,c=$\frac{0.5mol}{0.25L}$=2mol/L;从中取出1mL,其物质的量浓度不变,为2mol/L;n=cV=0.001L×2mol/L=0.002mol,m=nM=0.002mol×40g/mol=0.08g;溶液稀释前后溶质的物质的量不变,这1mL溶液用水稀释到100mL,所得溶液中溶质的物质的量浓度为$\frac{0.001L×2mol/L}{0.1L}$=0.02mol/L;其中含Na+的物质的量为:0.02mol/L×0.1L=0.002mol,质量为0.002mol×23g/mol=0.046g,
故答案为:2mol/L;2mol/L;0.08g;0.02mol/L;0.046g.
点评 本题考查物质的量浓度计算,题目难度不大,注意有关计算公式的运用,把握溶液的特点以及溶液稀释前后溶质的物质的量不变的特征

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
9.2015年8月12日天津塘沽发生大型爆炸事件造成多人伤亡,专家估测其能量不亚于24吨TNT(2、4、6-三硝基甲苯)爆炸发出的能量,同时现场发现有大量的碱、氰化钠等化学物质.下列说法正确的是( )
| A. | 爆炸一定都属于化学变化 | |
| B. |  盛放氰化钠的容器上应贴有如图所示的安全标识 | |
| C. | 生石灰烧伤应立即用大量的水冲洗并涂上中和剂硼酸 | |
| D. | TNT爆炸的产物只有CO、CO2及氮氧化物 |
13.如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略).
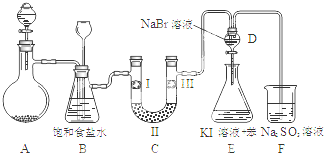
(1)制备氯气选用的药品为:漂粉精固体和浓盐酸,相关的化学反应方程式为:Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象锥形瓶中液面下降,长颈漏斗中液面上升.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入d.
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性.当向D中缓缓通入足量氯气时,可以看到无色溶液逐渐变为深棕红色,说明氯的非金属性大于溴.打开活塞,将装置D中少量溶液加入装置E中,振荡.观察到的现象是E中溶液分为两层,上层(苯层)为紫红色.该现象不能说明溴的非金属性强于碘 (填“能”或“不能”),原因是过量的Cl2也可将I-氧化为I2.

(1)制备氯气选用的药品为:漂粉精固体和浓盐酸,相关的化学反应方程式为:Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象锥形瓶中液面下降,长颈漏斗中液面上升.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入d.
| a | b | c | d | |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| II | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| III | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
14.设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,11.2 L SO3所含的氧原子数为1.5NA | |
| B. | 电解精炼铜时,若阳极质量减少6.4 g,则电路中转移电子数为0.2NA | |
| C. | 常温常压下,4.0 g CH4中含有共价键的数目为NA | |
| D. | 在含Al3+总数为NA的AlCl3溶液中,Cl-总数为3NA |
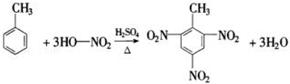 .
.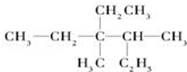 用系统命名法命名:3,4-二甲基-3-乙基己烷
用系统命名法命名:3,4-二甲基-3-乙基己烷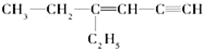 ,其中在同一平面上的碳原子至少为6个.
,其中在同一平面上的碳原子至少为6个.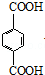 .
.