题目内容
3.下列物质分类的正确组合是( )| 选项 | 酸 | 碱 | 碱性氧化物 | 盐 |
| A | H2CO3 | 纯碱 | CaO | 明矾 |
| B | H2SO4 | 烧碱 | Na2O | 小苏打 |
| C | HNO3 | 氨水 | Al2O3 | 石灰石 |
| D | NaHCO3 | 熟石灰 | Al(OH)3 | 食盐 |
| A. | A | B. | B | C. | C | D. | D |
分析 酸是指在电离时产生的阳离子全部是氢离子的化合物;
碱是电离产生的阴离子全部为氢氧根离子的化合物;
碱性氧化物是指能和酸反应生成盐和水的化合物,反应为复分解反应;
盐是由金属离子和酸根离子组成的化合物;据此回答判断.
解答 解:A.纯碱为碳酸钠为盐,不是碱,故A错误;
B.硫酸为酸,烧碱为氢氧化钠为碱,氧化钠和酸反应生成盐和水为碱性氧化物,小苏打为碳酸氢钠为盐,故B正确;
C.氧化铝是两性氧化物,不是碱性氧化物,故C错误;
D.碳酸氢钠是盐不是酸,氢氧化铝不是氧化物,故D错误;
故选B.
点评 本题考查学生物质的分类知识,注意基本概念的理解和掌握是关键,题目难度中等.

练习册系列答案
相关题目
11.下列实验操作、现象及由此得出的结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将铜粉加入1.0mol•L-1Fe2(SO4)3溶液中 | 铜粉溶解 | 金属铜比铁活泼 |
| B | 将pH试纸放在玻片上,用玻璃棒蘸取某新制氯水,点在pH试纸中央,与标准比色卡对照 | pH=2 | 氯气与水反应生成了强酸 |
| C | 向含有Fe2+的MgSO4溶液中,先加H2O2溶液,然后再调溶液的pH约为5 | 有红褐色沉淀生成 | Fe2+被H2O2氧化为Fe3+ |
| D | 将KI和FeCl3溶液在试管中混合后,加入汽油,振荡,静置 | 下层溶液显紫红色 | 生成的I2全部溶于汽油中 |
| A. | A | B. | B | C. | C | D. | D |
18.下列有关实验操作和说法中,正确的是( )
| A. | 进行硫酸铜溶液的浓缩结晶实验需要的仪器主要有烧杯、玻璃棒、蒸发皿 | |
| B. | 用容量瓶配溶液时,若加水超过刻度线,立即用滴管吸出多余液体 | |
| C. | 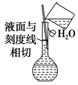 按图所示配制溶液 | |
| D. | 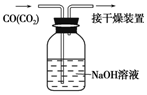 按如图可除去CO中混有的CO2 |
15.钛(Ti)被称为铁、铝之后的第二金属,以TiO2制取Ti的主要反应
①TiO2+2Cl2+2C$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO
②TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$2MgCl2+Ti
下列说法正确的是( )
①TiO2+2Cl2+2C$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO
②TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$2MgCl2+Ti
下列说法正确的是( )
| A. | 反应①是置换反应 | B. | 反应②是复分解反应 | ||
| C. | 反应①中TiO2是氧化剂 | D. | 反应②中金属镁是还原剂 |
12.常温下,下列各组离子一定能大量共存的是( )
| A. | 使甲基橙试液变红的溶液中:Al3+ Cu2+NO3-SO42- | |
| B. | pH>7的溶液中:Na+Mg2+SO42-I- | |
| C. | 由水电离出的c(H+)=l.0×10-13 mol•L-1的溶液中:Na+CO32-SO32-Cl- | |
| D. | 加铝粉能产生大量H2的溶液中:Na+NH4+NO3-Cl- |