题目内容
下列说法正确的是( )
| A、离子化合物中一定含有离子键 |
| B、含有共价键的化合物一定是共价化合物 |
| C、强电解质与弱电解质的划分标准是电解质在水溶液中导电能力的强弱 |
| D、氧气中氧元素的化合价为0,所以氧分子中没有化学键 |
考点:离子化合物的结构特征与性质,共价键的形成及共价键的主要类型,强电解质和弱电解质的概念
专题:
分析:A.含有离子键的化合物是离子化合物,离子化合物中一定含有离子键;
B.只含共价键的化合物是共价化合物,含有共价键的化合物可能是离子化合物;
C.根据电解质的电离程度将电解质划分为强弱电解质;
D.氧气分子中O原子之间存在共价键.
B.只含共价键的化合物是共价化合物,含有共价键的化合物可能是离子化合物;
C.根据电解质的电离程度将电解质划分为强弱电解质;
D.氧气分子中O原子之间存在共价键.
解答:
解:A.含有离子键的化合物是离子化合物,离子化合物中一定含有离子键,可能含有共价键,故A正确;
B.只含共价键的化合物是共价化合物,含有共价键的化合物可能是离子化合物,如KOH,故B错误;
C.根据电解质的电离程度将电解质划分为强弱电解质,溶液导电能力与离子浓度成正比,故C错误;
D.氧气分子中O原子之间存在共价键,因为氧气分子中共用电子对不偏离任何一方,所以其化合价为0,故D错误;
故选A.
B.只含共价键的化合物是共价化合物,含有共价键的化合物可能是离子化合物,如KOH,故B错误;
C.根据电解质的电离程度将电解质划分为强弱电解质,溶液导电能力与离子浓度成正比,故C错误;
D.氧气分子中O原子之间存在共价键,因为氧气分子中共用电子对不偏离任何一方,所以其化合价为0,故D错误;
故选A.
点评:本题考查化合物和化学键的关系、强弱电解质的判断、化学键与化合价的关系等知识点,综合性较强,会根据化合物中存在的化学键判断化合物类型,注意溶液导电性与电解质强弱无关,与离子所带电荷、离子浓度有关,为易错点.

练习册系列答案
相关题目
用铁棒与石墨棒做电极来电解饱和食盐水,电解前在食盐水中滴加酚酞试液,电解时下列叙述中正确的是( )
| A、铁棒连接直流电源的正极,石墨连接直流电源的负极 |
| B、溶液中的OH-离子向阳极移动,阳极周围显红色 |
| C、跟直流电源正极相连的电极上产生能使KI淀粉溶液变蓝的气体 |
| D、跟直流电源负极相连的电极上发生氧化反应,产生无色可以燃烧的气体 |
一个原电池的总反应为Zn+Cu2+=Zn2++Cu,该反应的原电池的正确组成是( )
| A、正极 Zn 负极 Cu 电解质溶液 CuCl2 |
| B、正极Cu 负极Zn 电解质溶液 CuCl2 |
| C、正极Zn 负极Cu 电解质溶液 ZnCl2 |
| D、正极Cu 负极Zn 电解质溶液 ZnCl2 |
同温同压下等体积的SO2与CO2气体,下列叙述错误的是( )
| A、两种气体中含有相同的质子数 |
| B、SO2与CO2的密度之比为16:11 |
| C、SO2与CO2的质量之比为16:11 |
| D、SO2与CO2含有的电子数之比为16:11 |
下列物质中,只含有极性共价键的是( )
| A、CaCl2 |
| B、KOH |
| C、H2 |
| D、H2O |
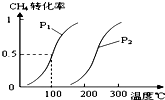 甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH4和H2O为原料来制备甲醇.
甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH4和H2O为原料来制备甲醇.