��Ŀ����
A��B��C��D��E���ֶ�����Ԫ�أ�AԪ�ص�������ɫ��ӦΪ��ɫ��B������������Ӧˮ����B��OH��25.8gǡ������100mL 2mol?L-1������ȫ��Ӧ����Bԭ�Ӻ�������������������ȣ�E2�ڻ���ɫ����C2��ȼ�ղ�����ɫ���森DԪ��ԭ�ӵ������������Ǵ�����������3����
�������������ش�
��1��CԪ�������ڱ��е�λ���� ��
��2��A��D�γɵ���ɫ������������к��еĻ�ѧ������Ϊ ��
��3��C2��ADE��Һ��Ӧ�����ӷ���ʽΪ ��
��4���õ���ʽ��ʾBC2���γɹ��� ��
��5����Ԫ��D��E���ɵ�9e-�������� ��
��6����KOH��ҺΪ�������Һ����D2��E2����ȼ�ϵ�أ������ķ�ӦʽΪ ��
�������������ش�
��1��CԪ�������ڱ��е�λ����
��2��A��D�γɵ���ɫ������������к��еĻ�ѧ������Ϊ
��3��C2��ADE��Һ��Ӧ�����ӷ���ʽΪ
��4���õ���ʽ��ʾBC2���γɹ���
��5����Ԫ��D��E���ɵ�9e-��������
��6����KOH��ҺΪ�������Һ����D2��E2����ȼ�ϵ�أ������ķ�ӦʽΪ
���㣺λ�ýṹ���ʵ����ϵӦ��
ר�⣺Ԫ����������Ԫ�����ڱ�ר��
������A��B��C��D��E���ֶ�����Ԫ�أ�AԪ�ص�������ɫ��ӦΪ��ɫ����AΪNa��B������������Ӧˮ����B��OH��25.8gǡ������100mL 2mol?L-1������ȫ��Ӧ����B�Ļ��ϼ�Ϊx��Ħ������Ϊy����
��x=0.2����Ȼx=2��y=24���ϣ�Bԭ�Ӻ�������������������ȣ���B��������Ϊ12����BΪMgԪ�أ���Bԭ�Ӻ�������������������ȣ���BΪMg��E2���������ڻ���ɫ����C2����������ȼ�ղ�����ɫ���棬��EΪH��CΪCl��DԪ��ԭ�ӵ������������Ǵ�����������3������DΪO���ݴ˽���С�⼴�ɣ�
| 5.8g |
| y+17x |
���
�⣺���ݷ�����֪��AΪNa��BΪMg��CΪCl��DΪO��EΪH��
��1��CΪCl��λ��Ԫ�����ڱ��е������ڵڢ���A�壬�ʴ�Ϊ���������ڵڢ���A�壻
��2��AD�ֱ�ΪNa��O�������γɹ������ƣ���������Ϊ����ɫ���壬���������к������Ӽ������ۼ����ʴ�Ϊ�����Ӽ������ۼ���
��3���������������Ʒ�Ӧ�����Ȼ��ơ��������ƺ�ˮ�����ӷ�Ӧ����ʽΪ��Cl2+2OH-=Cl-+ClO-+H2O���ʴ�Ϊ��Cl2+2OH-=Cl-+ClO-+H2O��
��4���Ȼ�þΪ���ӻ�������γɹ���Ϊ��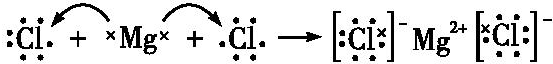
���ʴ�Ϊ��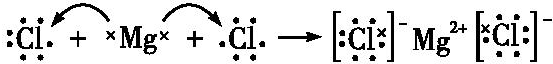 ��
��
��5��O��H���ɵ�9e-����-OH���������ǻ����ʴ�Ϊ���ǻ���
��6���������������ɵ�ȼ�ϵ���У������õ����ӣ�������ԭ��Ӧ���������ҺΪ���ԣ��ʲ���Ϊ������������O2+2H2O+4e-=4OH-���ʴ�Ϊ��O2+2H2O+4e-=4OH-��
��1��CΪCl��λ��Ԫ�����ڱ��е������ڵڢ���A�壬�ʴ�Ϊ���������ڵڢ���A�壻
��2��AD�ֱ�ΪNa��O�������γɹ������ƣ���������Ϊ����ɫ���壬���������к������Ӽ������ۼ����ʴ�Ϊ�����Ӽ������ۼ���
��3���������������Ʒ�Ӧ�����Ȼ��ơ��������ƺ�ˮ�����ӷ�Ӧ����ʽΪ��Cl2+2OH-=Cl-+ClO-+H2O���ʴ�Ϊ��Cl2+2OH-=Cl-+ClO-+H2O��
��4���Ȼ�þΪ���ӻ�������γɹ���Ϊ��
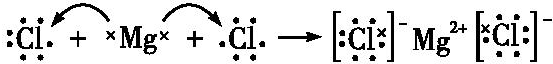
���ʴ�Ϊ��
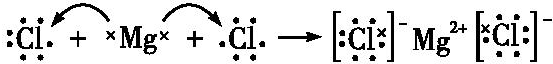 ��
����5��O��H���ɵ�9e-����-OH���������ǻ����ʴ�Ϊ���ǻ���
��6���������������ɵ�ȼ�ϵ���У������õ����ӣ�������ԭ��Ӧ���������ҺΪ���ԣ��ʲ���Ϊ������������O2+2H2O+4e-=4OH-���ʴ�Ϊ��O2+2H2O+4e-=4OH-��
���������⿼��λ�á��ṹ�����ʵĹ�ϵ��Ӧ�ã���ȷԪ�ص��ƶ��ǽ����Ĺؼ�����ϤԪ�ؼ��䵥�ʡ�����������ʼ��ɽ���ѶȲ���

��ϰ��ϵ�д�
 ������ÿ�ʱ�Ż���ҵϵ�д�
������ÿ�ʱ�Ż���ҵϵ�д�
�����Ŀ
��һ�������£����淴ӦX��g��+3Y��g��=2Z��g�� �ﵽ��Ӧ��ʱ����25%��Xת��ΪZ����37.5%��Yת��ΪZ����ʼʱ���������е�X��Y�����ʵ���֮��Ϊ��������
| A��1��2 | B��2��1 |
| C��1��3 | D��3��1 |
���з�Ӧ�����ӷ���ʽ��ȷ���ǣ�������
| A��пƬ������������Һ�У�Zn+Ag+�TZn2++Ag |
| B������������ˮ�Ʊ������Cl2+H2O�T2H++Cl-+ClO- |
| C�����������Ƽӵ���ˮ�У�Na+2H2O�TNa++OH-+H2�� |
| D��������ͭ�ӵ������У�Cu��OH��2+2H+�TCu2++2H2O |
