题目内容
(4分)在25℃时,有pH为a的HCl溶液和pH为b的NaOH溶液,取VaL该盐酸溶液用该NaOH溶液中和,需VbL NaOH溶液,(题中a≤b,b≥8)。问:
(1)若a+b=14,则Va/Vb= .
(2)若a+b=13,则Va/Vb=
(3)若a+b>14,则Va/Vb= ,且Va Vb(填“>”“<”“=”)
(1)、1 (2)、0.1或1/10 (3)、10a+b-14或10a+b-14>1、<
解析试题分析:根据水的离子积常数可知,氢氧化钠中OH-浓度是10b-14mol/L。酸碱恰好反应,所以有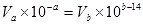 ,即Va/Vb=10a+b-14,所以(1)若a+b=14,则Va/Vb=1:1;(2)若a+b=13,则Va/Vb=1:10 ;(3)若a+b>14,由a+b=14+
,即Va/Vb=10a+b-14,所以(1)若a+b=14,则Va/Vb=1:1;(2)若a+b=13,则Va/Vb=1:10 ;(3)若a+b>14,由a+b=14+ 可推出:Va/Vb=10a+b-14>1则Va>Vb。
可推出:Va/Vb=10a+b-14>1则Va>Vb。
考点:考查溶液酸碱性的判断。

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
在下列变化过程中,被破坏的作用力正确的是
| A.干冰升华一一共价键 |
| B.二氧化硅熔融——范德华力 |
| C.氢氧化钠熔融——离子键、共价键 |
| D.硫酸氢钠溶于水——离子键、共价键 |
将纯水加热至较高温度,下列叙述正确的是
| A.水的离子积变大、pH变小、呈酸性 | B.水的离子积不变、pH不变、呈中性 |
| C.水的离子积变小、pH变大、呈碱性 | D.水的离子积变大、pH变小、呈中性 |
8分)阅读下列实验内容,根据题目要求回答问题。
实验室中有一未知浓度的稀盐酸,某学生用0.100mol·L-1 NaOH标准溶液进行测定盐酸的浓度的实验。取20.00 mL待测盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。请完成下列填空:
| 实验编号 | 待测盐酸的体积(mL) | NaOH溶液的浓度(mol·L-1) | 滴定完成时,NaOH溶液滴入的体积(mL) |
| 1 | 20.00 | 0.10 | 24.18 |
| 2 | 20.00 | 0.10 | 23.06 |
| 3 | 20.00 | 0.10 | 22.96 |
(2)根据上述数据,可计算出该盐酸的浓度约为 (保留小数点后叁位)。
(3)若滴定结束时,碱式滴定管中的液面如图所示,终点读数为 mL。
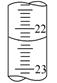
(4)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有 。
A.用酸式滴定管取20.00 mL待测盐酸,使用前,水洗后未用待测盐酸润洗
B.锥形瓶水洗后未干燥
C.称量NaOH固体时,有小部分NaOH潮解
D.滴定终点读数时俯视
E.碱式滴定管尖嘴部分有气泡,滴定后消失
(10分)某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作:
| A.在250 mL容量瓶中定容成250 mL烧碱溶液; |
| B.用碱式滴定管移取25 mL烧碱溶液于锥形瓶中并滴加几滴甲基橙作指示剂; |
| C.在天平上准确称取烧碱样品m g,在烧杯中加蒸馏水溶解; |
| D.将物质的量浓度为c mol·L-1的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度为V1 mL; |
回答下列问题:
(1)正确操作步骤的顺序是(用字母填写)
 D
D  。
。(2)操作D中液面应调整到 。
(3)滴定终点的现象是 。
(4)若酸式滴定管没有用标准H2SO4润洗,会对测定结果有何影响? (填“偏高”、“偏低”或“无影响”,其它操作均正确)。
(5)该烧碱样品的纯度计算式是 。
下列物质常温下为液态的是
| A.苯 | B.乙炔 | C.乙烯 | D.甲烷 |
下列关于甘氨酸(H2N-CH2-COOH)性质的说法中正确的是
| A.只有酸性,没有碱性 | B.只有碱性,没有酸性 |
| C.既有酸性,又有碱性 | D.既没有酸性,又没有碱性 |
下列实验仪器不能用于混合物分离提纯的是
| A.漏斗 | B.蒸馏烧瓶 | C.容量瓶 | D.分液漏斗 |