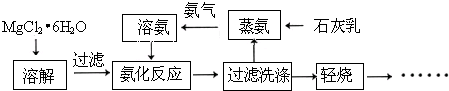
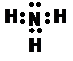��Ŀ����
��1����FeCl3��Һ�м���a g��ͭ�ۣ�����ʹ֮ȫ���ܽ⣬��Һ��һ���е���������_________�������е��������� ��������Ӧ�����ӷ���ʽΪ ���������м��� b g���ۣ���ַ�Ӧ����˵�����c g�����ܷ�����Ӧ�����ӷ���ʽΪ ������֪ a��b��c���� c��������_________��
��2������Na2SO3��Һ��ϡH2SO4���밴Ҫ������±���
|
���� |
���� |
������ |
|
1 |
�üס�����֧�Թֱܷ�ȡ������Һ�������� |
|
|
2 |
�ý�ͷ�ι�����Թ�����εμ�BaCl2��Һ�������� |
|
|
3 |
�� |
������� ������ �� ������� ������ �� |
˵������3������ʹ�������κ�������������ͷ�ιܣ����Լ���
��12�֣�
��1��Fe2+��Cu2+ Fe3+ Cu+2Fe3+=2Fe2++Cu2+
2Fe3+ + Fe= 3Fe2+ �� Fe+ Cu2+= Fe2+ + Cu Cu
��2�������Թ�����Һ������Թܣ��ӱ��� �����ݲ��� Na2SO3��Һ ϡH2SO4 �������ݲ����������д̼�����ζ����ų� ϡH2SO4 Na2SO3��Һ
��������
�����������1���Ȼ�����Һ������ͭ��Ϊ��ʹ֮��ȫ�ܽ⣬�Ȼ�����Һ���ܹ���������Cu+2Fe3+=2Fe2++Cu2+�����ܽ�ͭ�����Һ��һ�����еĽ���������ΪFe2+��Cu2+�������е���Fe3+�����������ԣ�Fe3+ >Cu2+>Fe2+�������һ����������ʱ���ȷ����ķ�ӦΪ2Fe3+ + Fe= 3Fe2+�������ӱ���ԭ���������ۻ����ٷ�����ӦFe+ Cu2+= Fe2+ + Cu������a>b>c��˵��������Һ�н���������һ������Fe2+��Cu2+����������п϶�û��Fe��ֻ��Cu����2����������2���Թ��з�ӦʽΪNa2SO3+BaCl2=BaSO3��+2NaCl��H2SO4+BaCl2=BaSO4��+2HCl����3������ʹ�������κ��������Լ���ֻ�ܽ����Թ�����Һ������Թܣ����������ܽ⣬�������ݲ����������Na2SO3��Һ������ϡH2SO4�����������ݣ��������ݲ����������ϡH2SO4������Na2SO3��Һ����ΪBaSO3��ϡH2SO4���������Ӧ���������ᱵ������SO2��H2O����ϡHCl��������Na2SO3��Ӧʱ��������������NaHSO3����������Na2SO3��Һ��Ӧʱ����SO2��
���㣺����Fe3+�������ԡ�Cu�Ļ�ԭ�ԡ�������ԭ��Ӧ���Ⱥ������ƶϡ����ʼ��鷽������ơ����ӷ���ʽ����д�����֪ʶ��

| A����Ba��NO3 ��2��Һ����Na2SO3��Na2SO4 | B����ȥ�����������ӣ��������м���������NaOH��Һ����� | C������ˮ��CCl4�����Һ©�������ã��ɽ�����ȡ��CCl4�� | D��ȡ0.1mol FeCl3��������ˮ����100mL����ƿ���ݺ�õ�1 mol?L-1FeCl3��Һ |