题目内容
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,1 mol H2O 的体积为22.4L |
| B、5.85g NaCl溶于1 L水形成溶液,所得溶液中溶质的物质的量浓度为0.1 mol/L |
| C、32 g O2 和32 g O3所含的原子数都为2NA |
| D、CO2的摩尔质量为44 g |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、标况下水为液态;
B、5.85gNaCl固体溶于1L水,所得溶液的体积将大于1L;
C、根据n=
并结合O2 和O3的分子组成来判断;
D、摩尔质量的单位为g/mol.
B、5.85gNaCl固体溶于1L水,所得溶液的体积将大于1L;
C、根据n=
| m |
| M |
D、摩尔质量的单位为g/mol.
解答:
解:A、标况下水为液态,故A错误;
B、5.85gNaCl固体溶于1L水,所得溶液的体积将大于1L,故溶液的浓度将小于0.1mol/L,故B错误;
C、32gO2的物质的量n=
=
=1mol,含有的氧原子的物质的量n=1mol×2=2mol,个数为2NA;32gO3的物质的量n=
=
=
mol,故含有的氧原子的物质的量n=
mol×3=2mol,个数为2NA,故C正确;
D、摩尔质量的单位为g/mol,故D错误.
故选C.
B、5.85gNaCl固体溶于1L水,所得溶液的体积将大于1L,故溶液的浓度将小于0.1mol/L,故B错误;
C、32gO2的物质的量n=
| m |
| M |
| 32g |
| 32g/mol |
| m |
| M |
| 32g |
| 48g/mol |
| 2 |
| 3 |
| 2 |
| 3 |
D、摩尔质量的单位为g/mol,故D错误.
故选C.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构是关键,难度不大.

练习册系列答案
相关题目
有机物的种类繁多,但其命中是有规则的.下列有机物命名正确的是( )
A、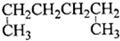 1,4-二甲基丁烷 1,4-二甲基丁烷 |
B、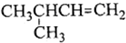 3-甲基丁烯 3-甲基丁烯 |
C、 2-甲基丁烷 2-甲基丁烷 |
| D、CH2Cl-CH2Cl 二氯乙烷 |
将淀粉与KI的混合液装在半透膜中,浸泡在盛有蒸馏水的烧杯中,过一段时间后,取烧杯中的液体进行实验,能证明半透膜有破损的是( )
| A、加入碘水不变蓝色 |
| B、加入碘水变蓝色 |
| C、加入AgNO3溶液不产生黄色沉淀 |
| D、加入AgNO3溶液产生黄色沉淀 |
下列物质属于糖类且属于高分子化合物的是( )
| A、蔗糖 | B、牛油 |
| C、纤维素 | D、蛋白质 |
某温度时,在体积为1L的密闭容器中,A、B、C三种气体浓度的变化如图I所示,若其它条件不变,当温度分别为Tl和T2时,B的体积百分含量与时间关系如图Ⅱ所示.则下列结论正确的是( )
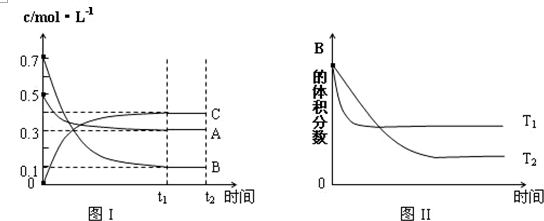

| A、该反应的热化学方程式为:A(g )+3B(g)?2C(g);△H>0 |
| B、达到平衡后,若其他条件不变,通入稀有气体,平衡向正反应方向移动 |
| C、达到平衡后,若其他条件不变,减小体积,平衡向逆反应方向移动 |
| D、若其它条件不变,升高温度,正、逆反应速率均增大,A的转化率减小 |
乙醇汽油(汽油中加入一定比例的乙醇)的使用可以缓解石油危机.从甜菜或甘蔗中提取的蔗糖可以通过发酵产生乙醇.下列过程中没有发生化学变化的是( )
| A、汽油中加入乙醇 |
| B、乙醇的燃烧 |
| C、蔗糖的发酵 |
| D、甜菜的生长 |
下列化学用语或模型图示正确的是( )
| A、HClO的结构式:H-Cl-O |
B、Na2O2的电子式: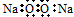 |
C、CO2的比例模型: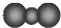 |
| D、Na原子外围电子排布式:3s1 |
下列实验设计、操作或实验现象均正确的是( )
| A、检验甲酸中是否混有甲醛,可向样品中加入足量NaOH溶液以中和HCOOH,再做银镜反应实验 |
| B、实验室制取乙酸乙酯时,将反应产生的蒸气经导管通入到饱和烧碱溶液中 |
| C、液态溴乙烷中加入AgNO3溶液观察有无淡黄色沉淀生成,以检验溴元素的存在 |
| D、实验室制硝基苯要在水浴的热水中插入温度计 |
关于氧化还原反应10AgF+5C12+5H2O═9口+AgClO3+10HF+O2,下列说法不正确的是( )
| A、每生成1 mol O2,该反应转移电子的物质的量是4NA | ||
| B、该反应中Cl2既是氧化剂,又是还原剂 | ||
| C、口中的物质是AgCl | ||
D、该反应消耗的水有
|