题目内容
17.某元素R有两种同位素10R与11R,已知R元素的近似相对原子质量为10.8,该元素的两种同位素原子的物质的量之比为( )| A. | 1:3 | B. | 1:4 | C. | 1:5 | D. | 2:3 |
分析 硼元素的相对原子质量是10.8,则硼元素的摩尔质量是10.8g/mol,再根据$\overline{M}$=$\frac{m总}{n总}$计算其物质的量之比.
解答 解:硼元素的相对原子质量是10.8,则硼元素的摩尔质量是10.8g/mol,设10B和11B的物质的量分别是xmol、ymol,则$\overline{M}$=$\frac{m总}{n总}$=$\frac{10g/mol×xmol+11g/mol×ymol}{(x+y)mol}$=10.8g/mol,解得:x:y=1:4,
故选B.
点评 本题考查物质的量的计算,难度不大.正确理解平均摩尔质量的计算方法是解本题关键.

练习册系列答案
相关题目
7.人体只能吸收Fe2+,而Fe2+很容易被氧化,所以服补铁剂时同时要服维生素C,说明维生素C具有( )
| A. | 氧化性 | B. | 碱性 | C. | 还原性 | D. | 酸性 |
8.下列有关叙述中正确的是( )
| A. | 同一弱电解质溶液,温度不同时,导电能力相同 | |
| B. | 强电解质的水溶液导电能力一定比弱电解质的水溶液导电能力强 | |
| C. | 强电解质在水溶液中的电离过程是不可逆的 | |
| D. | 易溶于水的电解质一定是强电解质 |
5.一定量的Fe与过量的盐酸反应制取氢气,下列措施中可加快反应速率的是( )
| A. | 加10mL水 | B. | 增大压强 | C. | 降低温度 | D. | CuSO4晶体 |
12.下列有关说法正确的是( )
| A. | 目前我国流通的硬币是由合金材料制成的 | |
| B. | Al与S直接化合可以得到Al2S3,则Fe与S直接化合也可以得到Fe2S3 | |
| C. | 黄铜耐腐蚀性强,不能与稀盐酸反应 | |
| D. | 某金(Au)合金的组成可表示为CuAu3.,其中金为-3价 |
10.下列有关物质的性质比较,错误的是( )
| A. | 非金属性:Cl>Br | B. | 金属性:Al>Mg | ||
| C. | 热稳定性:H2O>H2S | D. | 酸性:H3PO4>H3AsO4 |
8.有下列物质①白磷 ②金刚石 ③co2④二氧化硅 ⑤甲烷 ⑥四氯化碳 ⑦单质硅⑧铵离子,其分子结构或晶体结构单元中存在正四面体的是( )
| A. | 除③外 | B. | 只有①⑤⑥⑧ | C. | 除③⑧外 | D. | 除③④⑦⑧ |
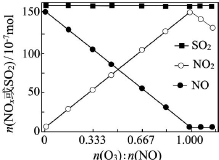 烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量.O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:
烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量.O3氧化烟气中SO2、NOx的主要反应的热化学方程式为: