题目内容
某研究小组为比较Al和Fe的金属性强弱,设计了图1所示的装置.

(1)甲中锥形瓶内盛放的液体是 .
(2)若要比较产生气体的快慢,可以比较相同时间内产生气体的体积,也可以比较 .
(3)为了确保“Al和Fe的金属活动性不同是导致产生气体速率不同的唯一原因”,实验时需要控制好反应条件.实验时除需保证甲中液体的体积、物质的量浓度和温度相同外,还需保证 .
(4)实验测得产生气体的速率(v)与时间(t)的关系如图2所示,则t1~t2时间内速率逐渐加快的主要原因是 ,t2~t3时间内速率逐渐减慢的主要原因是 .

(1)甲中锥形瓶内盛放的液体是
(2)若要比较产生气体的快慢,可以比较相同时间内产生气体的体积,也可以比较
(3)为了确保“Al和Fe的金属活动性不同是导致产生气体速率不同的唯一原因”,实验时需要控制好反应条件.实验时除需保证甲中液体的体积、物质的量浓度和温度相同外,还需保证
(4)实验测得产生气体的速率(v)与时间(t)的关系如图2所示,则t1~t2时间内速率逐渐加快的主要原因是
考点:常见金属的活动性顺序及其应用,性质实验方案的设计
专题:实验设计题
分析:(1)根据金属和酸反应的快慢判断金属性强弱;
(2)根据v=
分析;
(3)由外界条件对化学反应速率的影响分析;
(4)t1─t2阶段:金属与酸的反应为放热反应,温度影响化学反应速率;t2─t3阶段:随着反应的进行,酸的浓度降低反应减慢.
(2)根据v=
| △V |
| △t |
(3)由外界条件对化学反应速率的影响分析;
(4)t1─t2阶段:金属与酸的反应为放热反应,温度影响化学反应速率;t2─t3阶段:随着反应的进行,酸的浓度降低反应减慢.
解答:
解:(1)根据金属和酸反应置换氢的难易判断金属性强弱,故甲中应为稀盐酸或稀硫酸,故答案为:稀硫酸或稀盐酸;
(2)由v=
可知,反应速率与气体的体积和时间有关,所以一种是固定体积比较时间,另一种是固定时间比较体积,故答案为:产生相同体积的气体所需时间的长短;
(3)影响化学反应速率的因素有反应物的浓度、溶液的温度、固体的表面积等,所以还需保证Al和Fe表面积相同,故答案为:Al和Fe表面积相同;
(4)金属与酸的反应为放热反应,温度影响反应的速率,温度越高,反应的速率越快,随着反应的进行,溶液中盐酸的浓度不断减小,浓度越小反应速率越小.
故答案为:反应放热,溶液温度升高使反应速率加快;随着反应的进行,酸的浓度降低反应减慢.
(2)由v=
| △V |
| △t |
(3)影响化学反应速率的因素有反应物的浓度、溶液的温度、固体的表面积等,所以还需保证Al和Fe表面积相同,故答案为:Al和Fe表面积相同;
(4)金属与酸的反应为放热反应,温度影响反应的速率,温度越高,反应的速率越快,随着反应的进行,溶液中盐酸的浓度不断减小,浓度越小反应速率越小.
故答案为:反应放热,溶液温度升高使反应速率加快;随着反应的进行,酸的浓度降低反应减慢.
点评:本题考查了测气体的反应速率的方法,理解所学知识要点,通过比较、分析是解答的关键,注意外界条件影响化学反应速率,但决定化学反应速率的是物质本身的性质,题目难度中等.

练习册系列答案
相关题目
下列实验操作中,正确的是( )
| A、加热后的蒸发皿,要用坩埚钳夹取 | ||
| B、试管和烧杯都可以直接在火焰上加热 | ||
C、给试管里的液体加热,液体的体积一般不超过试管容积的
| ||
| D、用剩的药品不要乱丢,要放回原试剂瓶里 |
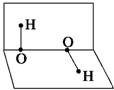 已知H2O2的分子空间结构可在二面角中表示,如图所示,则有关H2O2的结构的说法中不正确的是( )
已知H2O2的分子空间结构可在二面角中表示,如图所示,则有关H2O2的结构的说法中不正确的是( )| A、分子的正、负电荷重心不重合 |
| B、H2O2分子内既含极性键又含非极性键 |
| C、H2O2是极性分子 |
| D、H2O2分子间不可能形成氢键 |
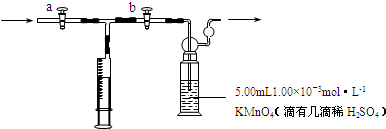
 为了证明铜与稀硝酸反应产生的是NO,某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,
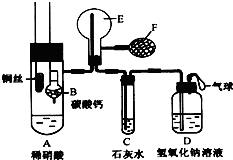
为了证明铜与稀硝酸反应产生的是NO,某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管, 合肥市某校化学兴趣小组为探究铁与浓硫酸反应,设计了如图所示装置进行实验.
合肥市某校化学兴趣小组为探究铁与浓硫酸反应,设计了如图所示装置进行实验.