题目内容
可逆反应达到平衡的根本原因是( )
| A、正逆反应的速率相等 |
| B、正逆反应都还在继续进行 |
| C、正逆反应的速率均为零 |
| D、反应混合物中各组分的浓度相等 |
考点:化学平衡状态的判断
专题:
分析:根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答:
解:A、化学平衡是动态平衡,当反应达到平衡状态时,正逆反应速率相等,这是达到平衡的根本原因,故A正确;
B、化学平衡是动态平衡,这是可逆反应的特征,故B错误;
C、化学平衡是动态平衡,正逆反应的速率均不为零,故C错误;
D、当体系达平衡状态时,反应混合物中各组分的浓度不变,而不是相等,故D错误;
故选A.
B、化学平衡是动态平衡,这是可逆反应的特征,故B错误;
C、化学平衡是动态平衡,正逆反应的速率均不为零,故C错误;
D、当体系达平衡状态时,反应混合物中各组分的浓度不变,而不是相等,故D错误;
故选A.
点评:本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
相关题目
下列说法中,错误的是( )
| A、向Na2SiO3溶液中通入CO2产生白色胶状沉淀 |
| B、NaOH溶液不能存放在磨口玻璃塞的试剂瓶中 |
| C、二氧化硅溶于水生成硅酸 |
| D、二氧化硅是一种熔沸点很高、硬度很大的氧化物 |
下列微粒中,只具有还原性的是( )
| A、Na+ |
| B、F2 |
| C、Cl- |
| D、SO32- |
下列说法中,正确的是:( )
①在水中氢、氧原子间均以化学键相结合.
②金属和非金属化合一定形成离子键.
③离子键的实质是阳离子、阴离子间的相互吸引.
④根据电离方程式HCl=H++Cl-,判断HCl分子里存在离子键.
⑤某些共价化合物中含有离子键.
①在水中氢、氧原子间均以化学键相结合.
②金属和非金属化合一定形成离子键.
③离子键的实质是阳离子、阴离子间的相互吸引.
④根据电离方程式HCl=H++Cl-,判断HCl分子里存在离子键.
⑤某些共价化合物中含有离子键.
| A、①②⑤正确 | B、都不正确 |
| C、③④正确 | D、仅⑤正确 |
下列离子方程式正确的是( )
| A、过氧化钠和水反应:2Na2O2+2H2O=4Na++4 OH-+O2↑ | ||||
B、用铜为电极电解饱和食盐水:2Cl-+2H2O
| ||||
| C、在明矾溶液中滴加过量氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O | ||||
| D、小苏打溶液中加少量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O |
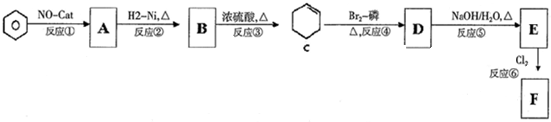
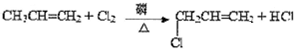 F的结构简式为
F的结构简式为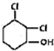
 直接制
直接制 ,理由是
,理由是