题目内容
已知乙醇的分子式为C2H6O,为了确定乙醇的结构是CH3OCH3还是CH3CH2OH,某化学兴趣实验小组设计了如下装置的实验(图中固定、夹持装置略去)
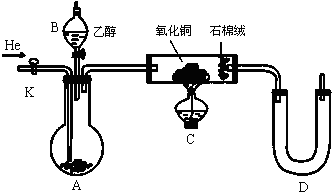
实验步骤如下:
①连接好装置,检验装置的气密性;
②盛装试剂,A中装入足量金属钠,C中装入足量氧化铜,B中装入59ml密度为0.78g/cm3的乙醇,D中装入相应试剂后称重为m1 g,连接好装置;
③打开活塞K通入一会儿氦气,后关闭活塞K;
④点燃C 处酒精灯,加热一段时间后,再将B处活塞打开,慢慢滴下乙醇,待乙醇全部放下后,关闭B处活塞;
⑤打开活塞K,缓慢通入一会儿氦气,后关闭活塞K;
⑥停止加热,拆卸装置,称量D的质量为m2 g.
试回答下列问题:
(1)B仪器的名称是 ;
(2)实验过程中,A处实验现象为 .
(3)当m2-m1= 时,乙醇的结构简式为CH3CH2OH,A处发生化学的方程式为 .
(4)下列有关实验的说法中正确的是 (选填序号)
a.可将通入的氦气换成通入空气
b.可将氧化铜换成氧化铁
c.装置D中可盛装浓硫酸、无水CaCl2、碱石灰
d.若所用金属钠少量被氧化时,不会影响D中的质量变化.

实验步骤如下:
①连接好装置,检验装置的气密性;
②盛装试剂,A中装入足量金属钠,C中装入足量氧化铜,B中装入59ml密度为0.78g/cm3的乙醇,D中装入相应试剂后称重为m1 g,连接好装置;
③打开活塞K通入一会儿氦气,后关闭活塞K;
④点燃C 处酒精灯,加热一段时间后,再将B处活塞打开,慢慢滴下乙醇,待乙醇全部放下后,关闭B处活塞;
⑤打开活塞K,缓慢通入一会儿氦气,后关闭活塞K;
⑥停止加热,拆卸装置,称量D的质量为m2 g.
试回答下列问题:
(1)B仪器的名称是
(2)实验过程中,A处实验现象为
(3)当m2-m1=
(4)下列有关实验的说法中正确的是
a.可将通入的氦气换成通入空气
b.可将氧化铜换成氧化铁
c.装置D中可盛装浓硫酸、无水CaCl2、碱石灰
d.若所用金属钠少量被氧化时,不会影响D中的质量变化.
考点:性质实验方案的设计
专题:实验设计题
分析:(1)根据装置中的仪器分析;
(2)A处的反应为钠与乙醇反应,根据钠的密度及其反应原理分析实验现象;
(3)根据乙醇的量计算生成氢气的量,再根据氢气还原氧化铜产生水的质量来分析;
(4)a.根据氦气的作用分析;
b.根据实验目的分析;
c.装置D是装固体干燥剂的;
d.根据实验原理目的分析.
(2)A处的反应为钠与乙醇反应,根据钠的密度及其反应原理分析实验现象;
(3)根据乙醇的量计算生成氢气的量,再根据氢气还原氧化铜产生水的质量来分析;
(4)a.根据氦气的作用分析;
b.根据实验目的分析;
c.装置D是装固体干燥剂的;
d.根据实验原理目的分析.
解答:
解:(1)B仪器的名称是分液漏斗,故答案为:分液漏斗;
(2)A处的反应为钠与乙醇反应生成乙醇钠和氢气,又钠的密度比乙醇大,所以实验现象为产生气泡,金属钠沉在溶液底部,故答案为:产生气泡,金属钠沉在溶液部;
(3)根据题意,乙醇的物质的量为
=1mol,则根据2Na+2C2H5OH→2C2H5ONa+H2↑,所以生成的氢气为0.5mol,再根据C中的反应,量计算生成氢气的量,再根据氢守恒还原氧化铜产生0.5mol水,所以m2-m1=0.5×18=9g,
故答案为:9;2Na+2C2H5OH→2C2H5ONa+H2↑;
(4)a.因为空气中含有水蒸气,对D的质量差会产生误差,故a错误;
b.可将氧化铜换成氧化铁,不影响氢气还原生成水的量,故b正确;
c.装置D是固体干燥剂,不能盛装浓硫酸,故c错误;
d.若所用金属钠少量被氧化时,因为氧化钠不与乙醇反应,所以不会影响D中的质量变化,故d正确;
故选:bd.
(2)A处的反应为钠与乙醇反应生成乙醇钠和氢气,又钠的密度比乙醇大,所以实验现象为产生气泡,金属钠沉在溶液底部,故答案为:产生气泡,金属钠沉在溶液部;
(3)根据题意,乙醇的物质的量为
| 59ml×0.78g/cm3 |
| 46g/mol |
故答案为:9;2Na+2C2H5OH→2C2H5ONa+H2↑;
(4)a.因为空气中含有水蒸气,对D的质量差会产生误差,故a错误;
b.可将氧化铜换成氧化铁,不影响氢气还原生成水的量,故b正确;
c.装置D是固体干燥剂,不能盛装浓硫酸,故c错误;
d.若所用金属钠少量被氧化时,因为氧化钠不与乙醇反应,所以不会影响D中的质量变化,故d正确;
故选:bd.
点评:本题考查了有机物乙醇分子组成的确定,题目难度中等,注意掌握常见有机物结构与性质,弄清钠与乙醇反应的本质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、常温常压下,8g O2含有0.5 NA个电子 |
| B、0.1mol/L NaOH溶液中含有OH一的数目为0.1 NA |
| C、标准状况下,22.4L盐酸含有NA个HCl分子 |
| D、常温常压下,14 g 由N2与CO组成的混合气体含有的原子数目为NA |
由氨气和氢气组成的混合气体的平均相对分子质量为12,则氨气和氢气的物质的量之比为( )
| A、1:1 | B、1:2 |
| C、2:1 | D、3:1 |
NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、1L 0.1 mol?L-1 NaCl溶液中含0.1NA个Na+ |
| B、22.4L NH3含4NA个原子 |
| C、标准状况下,22.4L H2O中含有10NA个电子 |
| D、NA个SO2分子的质量为64 g/mol |