题目内容
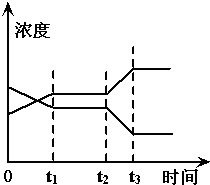 现有反应X(g)+Y(g)?2Z(g),△H>0.右图表示从反应开始到t1s时达到平衡,在t2s时由于条件变化使平衡破坏,到t3 s时又达平衡.则在图中t2 s时改变的条件可能是( )
现有反应X(g)+Y(g)?2Z(g),△H>0.右图表示从反应开始到t1s时达到平衡,在t2s时由于条件变化使平衡破坏,到t3 s时又达平衡.则在图中t2 s时改变的条件可能是( )| A、增大压强 |
| B、使用了催化剂 |
| C、升高温度 |
| D、减小了X或Y的浓度 |
考点:化学平衡建立的过程,化学平衡的影响因素
专题:化学平衡专题
分析:根据图可知,在t2 s时,反应物浓度减小,生成物浓度增大,说明平衡向正反应方向移动,而该反应为气体体积不变的吸热反应,据此答题.
解答:
解:根据图可知,在t2 s时,反应物浓度减小,生成物浓度增大,说明平衡向正反应方向移动,而该反应为气体体积不变的吸热反应,
A、增大压强,平衡不移动,故A错误;
B、使用催化剂平衡也不移动,故B错误;
C、升高温度,平衡正向移动,故C正确;
D、减小X或Y的浓度,平衡逆向移动,故D错误;
故选C.
A、增大压强,平衡不移动,故A错误;
B、使用催化剂平衡也不移动,故B错误;
C、升高温度,平衡正向移动,故C正确;
D、减小X或Y的浓度,平衡逆向移动,故D错误;
故选C.
点评:本题主要考查影响平衡移动的因素,难度不大,解题的关键在于根据图分析出t2 s时平衡移动的方向.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
H2SO3、H2CO3分别属于中强酸和弱酸,H2SO3?H++HSO3-,HSO3-?H++SO32-;H2CO3?H++HCO3-;HCO3-?H++CO32-;电离平衡常数分别为k1、k1′、k2、k2′,已知k1>k1′≈k2>k2′,则溶液中不可以大量共存的离子组合是( )
| A、SO32-、HCO3- |
| B、HSO3-、CO32- |
| C、SO32-、CO32- |
| D、HSO3-、HCO3- |
下列事实不能用勒夏特列原理解释的是( )
| A、溴水中有下列平衡:Br2+H2O?HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅 |
| B、反应 CO+NO2?CO2+NO (△H<0),达平衡后,提高温度体系颜色变深 |
| C、对于 2 HI?H2+I2 达平衡后,缩小体积可使体系颜色变深 |
| D、合成氨反应,为提高氨的产率,理论上应采取降低温度的措施 |
100mL 6mol/L H2SO4跟过量锌粉反应,恒温下,为减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量某物质或溶液,其中不能达到目的是( )
| A、醋酸钠(固体) |
| B、水 |
| C、硫酸钾溶液 |
| D、硫酸铵(固体) |
在一定条件下,向2L密闭容器中充入3mol X(g)和1mol Y(g)进行反应:2X(g)+Y(g)?3Z(g)+2W(g),某时刻测定产物的浓度,不可能的是( )
| A、Z=0.75mol/L |
| B、Z=1mol/L |
| C、W=1mol/L |
| D、Z=0.8mol/L |
下列电极反应式正确的是( )
| A、氯碱工业电解饱和食盐水时,阳极电极反应式为 2Cl--2e-=Cl2↑ |
| B、精炼铜时,与电源正极相连的是纯铜,电极反应式为 Cu-2e-=Cu2+ |
| C、氢氧燃料电池的负极反应式 O2+2H2O+4e-=4OH- |
| D、钢铁发生电化腐蚀的正极反应式 Fe-2e-=Fe2+ |
下列说法不正确的是( )
| A、一个反应能否自发进行取决于该反应放热还是吸热 |
| B、同一条件下不同物质有不同的熵值,其体系的混乱程度越大,熵值越大 |
| C、焓变是一个与反应能否自发进行有关的因素,多数能自发进行的反应都是放热反应 |
| D、一个反应能否自发进行,与焓变和熵变的共同影响有关 |