题目内容
同温同压下,将充有NO2、NO和O2的大试管倒置于水中,片刻之后水溶液充满整个大试管,则反应前NO2、NO和O2的体积比可能是( )
| A、1:1:1 |
| B、4:24:5 |
| C、4:24:7 |
| D、4:24:19 |
考点:有关混合物反应的计算
专题:
分析:若气体能完全溶于水,即NO、NO2、O2三种气体恰好完全反应,全部生成了硝酸,根据反应中电子得失守恒,应该有n(NO)×3+n(NO2)=n(O2)×4,据此对各选项进行判断.
解答:
解:若气体能完全溶于水,即NO、NO2、O2三种气体恰好完全反应,全部生成了硝酸,在反应中1molNO失去3mol电子,1molNO2失去1mol电子,1molO2得到4mol电子生成HNO3,根据反应中电子得失守恒,应该有:n(NO2)+n(NO)×3=n(O2)×4成立,相同条件下气体体积与物质的量成正比,则:V(NO2)+V(NO)×3=V(O2)×4,
A.1+1×3=4≠1×4,故A错误;
B.4+24×3≠5×4,故B错误;
C.4+24×3≠7×4,故C错误;
D.4+24×3=76=19×4,故D正确;
故选D.
A.1+1×3=4≠1×4,故A错误;
B.4+24×3≠5×4,故B错误;
C.4+24×3≠7×4,故C错误;
D.4+24×3=76=19×4,故D正确;
故选D.
点评:本题主要考查了混合物反应的计算,侧重氧化还原反应中的电子守恒,题目难度中等,掌握反应中电子得失守恒是解题的关键,试题侧重分析能力和计算能力的考查.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
将甲烷、氧气、过氧化钠置于密闭容器中,在150℃时用电火花点燃,充分反应后容器内压强为零,则甲烷、氧气、过氧化钠的物质的量之比为( )
| A、1:2:3 |
| B、2:1:6 |
| C、2:1:3 |
| D、1:2:6 |
下列说法正确的是( )
| A、c(H+)>1.0×10-71mol?L-1的溶液一定呈酸性 |
| B、c(H+)?c(OH-)=1.0×10-14的溶液一定呈中性 |
| C、中性溶液中的c(H+)一定等于1.0×10-71mol?L-1 |
| D、c(H+)=c(OH-)的溶液一定是中性溶液 |
下列说法正确的是( )
| A、PM2.5的产生与人类活动无关 |
| B、在涂料中尽量用液态有机物代替水作溶剂,以减少环境污染 |
| C、酒精可使蛋白质变性,故能消毒杀菌 |
| D、塑化剂是一种化工塑料添加剂,可以大量添加到婴幼儿玩具中 |
下列有关核外电子运动规律的描述中,错误的是( )
| A、核外电子质量很小,在原子核外做高速运动 |
| B、在电子云示意图中,小黑点密表示电子在核外空间单位体积内出现的几率大 |
| C、在电子云示意图中,通常用小黑点来表示电子绕核做高速圆周运动 |
| D、s电子的原子轨道都是球形的,p电子的原子轨道都是哑铃形的 |
下下列说法可以证明反应N2+3H2?2NH3已达平衡状态的是( )
| A、1molN≡N键断裂的同时,有3molH-H键形成 |
| B、1molN≡N键断裂的同时,有3molH-H键断裂 |
| C、1molN≡N键断裂的同时,有3molN-H键断裂 |
| D、1molN≡N键断裂的同时,有6molN-H键形成 |
下列装置能构成原电池的是( )
A、 酒精 |
B、 AgNO3溶液 |
C、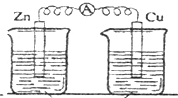 稀H2SO4 |
D、 稀H2SO4 |