题目内容
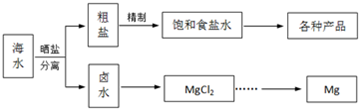
海洋中有丰富的食品、矿产、能源、药物和水产资源等(如图所示),下列有关说法正确的是( )


| A、第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入药品的顺序为Na2CO3、NaOH、BaCl2和盐酸 |
| B、第②步中结晶出的MgCl2?6H2O可在空气中受热分解制无水MgCl2 |
| C、在第③④⑤步中溴元素均被氧化 |
| D、由海水提取的金属镁能与金属铝、氢氧化钠溶液在一定条件下形成原电池,金属镁作该原电池正极 |
考点:海水资源及其综合利用
专题:元素及其化合物
分析:A、选项中的试剂添加顺序中,钡离子最后无法除去;
B、氯化镁晶体脱水过程中镁离子易水解生成氢氧化镁沉淀,在氯化氢气体中脱水可以抑制镁离子水解;
C、第④步中,溴元素被还原;
D、铝能够和氢氧化钠溶液发生氧化还原反应,镁不和氢氧化钠反应.
B、氯化镁晶体脱水过程中镁离子易水解生成氢氧化镁沉淀,在氯化氢气体中脱水可以抑制镁离子水解;
C、第④步中,溴元素被还原;
D、铝能够和氢氧化钠溶液发生氧化还原反应,镁不和氢氧化钠反应.
解答:
解:A、选项中的试剂添加顺序中,钡离子最后无法除去,加入的药品顺序应为:BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸,故A错误;
B、工段②中的MgCl2?6H2O脱水过程中镁离子易水解生成氢氧化镁沉淀,在氯化氢气体中脱水可以抑制镁离子水解;MgCl2?6H20要在HCl氛围中加热脱水制得无水MgCl2,故B错误;
C、在工段③、④、⑤中,第④步中,SO2+2H2O+Br2=H2SO4+2HBr中S元素的化合价升高,则二氧化硫被氧化,溴元素被还还原,故C错误;
D、铝能够和氢氧化钠溶液发生氧化还原反应失电子,作负极,镁作正极,故D正确.
故选:D.
B、工段②中的MgCl2?6H2O脱水过程中镁离子易水解生成氢氧化镁沉淀,在氯化氢气体中脱水可以抑制镁离子水解;MgCl2?6H20要在HCl氛围中加热脱水制得无水MgCl2,故B错误;
C、在工段③、④、⑤中,第④步中,SO2+2H2O+Br2=H2SO4+2HBr中S元素的化合价升高,则二氧化硫被氧化,溴元素被还还原,故C错误;
D、铝能够和氢氧化钠溶液发生氧化还原反应失电子,作负极,镁作正极,故D正确.
故选:D.
点评:本题考查了海水的综合利用,结合图象信息利用所学知识即可解答本题,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
化学与社会、生产、生活密切相关.下列说法正确的是( )
| A、石英只能用于生产光导纤维 |
| B、从海水提取物质都必须通过化学反应才能实现 |
| C、二氧化硫可广泛用于食品的漂白 |
| D、次氯酸钠溶液可用于环境的消毒杀菌 |
下列关于化学电源的说法正确的是( )
| A、干电池放电之后还能再充电 |
| B、充电电池在放电和充电时都是将化学能转化为电能 |
| C、充电电池可以无限制地反复放电、充电 |
| D、氢氧燃料电池是一种环境友好电池 |
已知空气-锌电池的电极反应:锌片:Zn-2OH--2e-═ZnO+H2O,石墨:
O2+H2O+2e-═2OH-据次推断锌片是( )
| 1 |
| 2 |
| A、负极,被氧化 |
| B、负极,被还原 |
| C、正极,被氧化 |
| D、正极,被还原 |
CO2转化成有机物实现碳循环,是解决温室效应的有效途径之一,此反应化学平衡常数的表达式为:K=
且温度升高,K值变小.下列说法正确的是( )
| c(CH3OH).c(H2O) |
| c3(H2).c(CO2) |
| A、该反应的化学方程式为3H2(g)+CO2(g)?CH3OH(g)+H2O(g)△H>O |
| B、在恒温、恒容的密闭容器中,混合气体的密度不再改变时,该反应一定达到平衡状态 |
| C、在恒温、恒容的密闭容器中,增大H2的浓度时,CO2的转化率增大 |
| D、平衡时,其他条件不变,使用催化剂有利用于CO2的转化 |
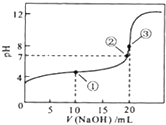 常温下,用0.1000mol/LNaOH溶液滴定20.00mL0.1000mol/LHCl溶液,滴定曲线如图所示,下列说法正确的是( )
常温下,用0.1000mol/LNaOH溶液滴定20.00mL0.1000mol/LHCl溶液,滴定曲线如图所示,下列说法正确的是( )| A、a=20.0 |
| B、滴定过程中,不可能存在:c(Cl-)>c(H)+>c(Na+)>c(OH-) |
| C、若用酚酞作指示剂,当滴定到溶液明显由无色变为红色时停止滴定 |
| D、若将盐酸换作同浓度的醋酸,则滴定到pH=7时,a>20.00 |
下列说法正确的是( )
| A、含5个碳原子的有机物,每个分子中最多可形成4个C-C单键 |
| B、油脂都不能使溴的四氯化碳溶液褪色 |
| C、可用新制的氢氧化铜悬浊液检验淀粉是否水解完全 |
| D、煤油可由石油分馏获得,可用作燃料和保存少量金属钠 |