题目内容
下列各图所示装置属于原电池的是( )
A、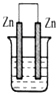 NaCl溶液 |
B、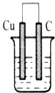 HCl溶液 |
C、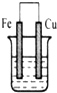 CuSO4溶液 |
D、 蔗糖溶液 |
考点:原电池和电解池的工作原理
专题:
分析:根据原电池的构成条件分析,原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应.
解答:
解:A.两个电极材料相同,所以不能构成原电池,故A错误;
B.该反应不能自发进行,所以不能构成原电池,故B错误;
C.该装置符合原电池构成条件,Fe易失电子作负极、C作正极,故C正确;
D.该装置中蔗糖不是电解质,该装置不能自发发生氧化还原反应,所以不能构成原电池,故D错误;
故选C.
B.该反应不能自发进行,所以不能构成原电池,故B错误;
C.该装置符合原电池构成条件,Fe易失电子作负极、C作正极,故C正确;
D.该装置中蔗糖不是电解质,该装置不能自发发生氧化还原反应,所以不能构成原电池,故D错误;
故选C.
点评:本题考查了原电池原理,明确原电池构成条件即可解答,这几个条件必须同时具备才能构成原电池,否则不能构成原电池.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
C5H12有3种不同结构:甲、CH3( CH2 )3CH3,乙、CH3CH (CH3 ) CH2CH3,丙、C(CH3)4.下列相关叙述正确的是( )
| A、甲、乙、丙属同系物,均可与氯气发生取代反应 |
| B、甲的分子中所有碳原子在同一直线上 |
| C、甲、乙、丙中,丙的沸点最低 |
| D、丙有3种不同沸点的二氯取代物 |
将1mol A(g)和2mol B(g)置于2L某密闭容器中,在一定温度下发生反应:
A(g)+B(g)?C(g)+D(g),并达到平衡.C的体积分数随时间变化如图Ⅰ中曲线b所示,反应过程中的能量变化如图Ⅱ所示,下列说法不正确的是( )
A(g)+B(g)?C(g)+D(g),并达到平衡.C的体积分数随时间变化如图Ⅰ中曲线b所示,反应过程中的能量变化如图Ⅱ所示,下列说法不正确的是( )

| A、反应在第4秒钟达到化学平衡状态,0~4秒内,以A表示的化学反应速率是 0.225 mol?L-1?s-1 |
| B、该温度下,压缩气体体积至1L,反应的平衡常数增大 |
| C、恒温条件下,缩小反应容器体积可以使反应的过程按图Ⅰ中a曲线进行 |
| D、在上述反应体系中加入催化剂,化学反应速率增大,则E1和E2均减小 |
已知反应A+3B═2C+D在某段时间内以A的浓度变化表示的化学反应速率为2mol?L-1?s-1,则此段时间内用B的浓度变化表示的化学反应速率为( )
| A、5 mol?L-1?s-1 |
| B、6 mol?L-1?s-1 |
| C、2 mol?L-1?s-1 |
| D、3 mol?L-1?s-1 |
 关于下列各图的叙述不正确的是( )
关于下列各图的叙述不正确的是( )| 表 丙 | |
| 化学方程式 | 平衡常数K |
| F2+H2?2HF | 6.5×1095 |
| Cl2+H2=2HCl | 2.6×1033 |
| Br2+H2?2HBr | 1.9×1019 |
| I2+H2?2HI | 8.7×102 |
| A、已知1molCO燃烧放出的热为283kJ,2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol则图甲表示CO和H2O(g)生成CO2和H2的能量变化 | ||
| B、某温度下,pH=11的NH3?H2O和pH=1的盐酸等体积混合后(不考虑混合后溶液体积的变化)恰好完全反应,反应后的溶液中NH4+、NH3?H2O与NH3三种微粒的平衡浓度之和为0.045mol?Lˉ1 | ||
| C、在常温下,X2(g)和H2反应生成HX的平衡常数如表丙所示,仅依据K的变化,就可以说明在相同条件下,平衡时X2(从F2到I2)的转化率逐减小,且X2与H2反应的剧烈程度逐渐减弱 | ||
D、图乙中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,
|
用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A、24g NaH中阴离子所含电子总数为NA |
| B、1mol苯分子中含有3NA个碳碳单键 |
| C、NO2和H2O反应毎生成2mol HNO3时转移的电子数目为2NA |
| D、在0.1mol/LK2CO3溶液中,阴离子数目大于0.1NA |
逻辑推理是化学学习中常用的一种思维方法,以下推理中正确的是( )
| A、单质都是由同种元素组成的,只含一种元素的物质一定是纯净物 |
| B、金属铝排在金属活动性顺序表中氢元素的前面,铝与酸反应一定放出氢气 |
| C、中和反应都有盐和水生成,有盐和水生成的反应都属于中和反应 |
| D、氧化物中都含有氧元素,含氧元素的化合物不一定是氧化物 |