题目内容
A、B、C、D、E、F为前四周期元素且原子序数依次增大.A的单质为密度最小的气体,A、D位于同一主族;B和C两种元素在周期表中位置相邻,在不同条件下可形成BC和BC2两种气态化合物;E的最外层电子数是C的价电子数的一半;F属于过渡元素,是日常生活中应用最广泛的金属之一,且有几种不同价态的氧化物,其中一种有磁性.
(1)E单质的晶体类型是 .
(2)C、D两种元素组成的具有非极性键的物质的电子式是 .
(3)F基态原子的电子排布式是 ,其+2价氧化物和E单质在高温下反应的化学方程式是 .
(4)由A、B、C三种元素形成的离子化合物溶于水后,溶液的pH (填大于,等于或小于)7,溶液中各离子浓度由大到小顺序为 .
(5)在25℃,101kPa下,单质A在氧气中燃烧后恢复至原温度和压强,每转移 1mol电子放出QkJ的热量,则单质A燃烧的热化学方程式是 .
(1)E单质的晶体类型是
(2)C、D两种元素组成的具有非极性键的物质的电子式是
(3)F基态原子的电子排布式是
(4)由A、B、C三种元素形成的离子化合物溶于水后,溶液的pH
(5)在25℃,101kPa下,单质A在氧气中燃烧后恢复至原温度和压强,每转移 1mol电子放出QkJ的热量,则单质A燃烧的热化学方程式是
考点:位置结构性质的相互关系应用
专题:
分析:A、B、C、D、E、F为前四周期元素且原子序数依次增大.A的单质为密度最小的气体,则A为氢元素,B和C两种元素在周期表中位置相邻,在不同条件下可形成BC和BC2两种气态化合物,则B为氮元素,C为氧元素;F属于过渡元素,是日常生活中应用最广泛的金属之一,且有几种不同价态的氧化物,其中一种有磁性,则F为铁元素,E的最外层电子数是C的价电子数的一半,则E为铝元素,A、D位于同一主族;且D的原子序数小于E,所以D为钠元素,据此答题.
解答:
解:A、B、C、D、E、F为前四周期元素且原子序数依次增大.A的单质为密度最小的气体,则A为氢元素,B和C两种元素在周期表中位置相邻,在不同条件下可形成BC和BC2两种气态化合物,则B为氮元素,C为氧元素;F属于过渡元素,是日常生活中应用最广泛的金属之一,且有几种不同价态的氧化物,其中一种有磁性,则F为铁元素,E的最外层电子数是C的价电子数的一半,则E为铝元素,A、D位于同一主族;且D的原子序数小于E,所以D为钠元素,
(1)E为铝元素,E单质的晶体类型是金属晶体,
故答案为:金属晶体;
(2)C、D两种元素组成的具有非极性键的物质为过氧化钠,它的电子式是 ,
,
故答案为: ;
;
(3)F为铁元素,原子序数为26,F基态原子的电子排布式是1s22s22p63s23p63d64s2(或[Ar]3d64s2),其+2价氧化物和铝单质在高温下发生铝热反应,反应的化学方程式是 2Al+3FeO
Al2O3+3Fe,
故答案为:1s22s22p63s23p63d64s2(或[Ar]3d64s2);2Al+3FeO
Al2O3+3Fe;
(4)由A、B、C三种元素形成的离子化合物为硝酸铵,硝酸铵溶于水后,由于铵根离子水解使溶液的pH小于7,溶液中各离子浓度由大到小顺序为c(NO3-)>c(NH4+)>c(H+)>c(OH-),
故答案为:小于;c(NO3-)>c(NH4+)>c(H+)>c(OH-);
(5)在25℃,101kPa下,氢气在氧气中燃烧后恢复至原温度和压强,每转移 1mol电子即有0.5mol氢气参加反应可以放出QkJ的热量,则氢气燃烧的热化学方程式是2H2(g)+O2 (g)=2H2O(l)△H=-4QKJ/mol,
故答案为:2H2(g)+O2 (g)=2H2O(l)△H=-4QKJ/mol;
(1)E为铝元素,E单质的晶体类型是金属晶体,
故答案为:金属晶体;
(2)C、D两种元素组成的具有非极性键的物质为过氧化钠,它的电子式是
 ,
,故答案为:
 ;
;(3)F为铁元素,原子序数为26,F基态原子的电子排布式是1s22s22p63s23p63d64s2(或[Ar]3d64s2),其+2价氧化物和铝单质在高温下发生铝热反应,反应的化学方程式是 2Al+3FeO
| ||
故答案为:1s22s22p63s23p63d64s2(或[Ar]3d64s2);2Al+3FeO
| ||
(4)由A、B、C三种元素形成的离子化合物为硝酸铵,硝酸铵溶于水后,由于铵根离子水解使溶液的pH小于7,溶液中各离子浓度由大到小顺序为c(NO3-)>c(NH4+)>c(H+)>c(OH-),
故答案为:小于;c(NO3-)>c(NH4+)>c(H+)>c(OH-);
(5)在25℃,101kPa下,氢气在氧气中燃烧后恢复至原温度和压强,每转移 1mol电子即有0.5mol氢气参加反应可以放出QkJ的热量,则氢气燃烧的热化学方程式是2H2(g)+O2 (g)=2H2O(l)△H=-4QKJ/mol,
故答案为:2H2(g)+O2 (g)=2H2O(l)△H=-4QKJ/mol;
点评:本题考查无机物的推断以及元素周期表与周期律的综合应用,题目考查角度较多,题目难度中等,注意把握相关物质的性质,正确推断元素为解答该题的关键.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
已知34Se、35Br位于同一周期,根据元素在周期表中的位置,判断下列说法正确的是( )
| A、离子还原性:Cl->Br- |
| B、气态氢化物的稳定性:H2S>H2Se |
| C、原子半径:Cl>Br>Se |
| D、酸性:H2SeO4>HBrO4>HClO4 |
 标准状况下,向100mLNaOH溶液中缓慢通入一定量的CO2气体,充分反应后,测得最后所得溶液显碱性(反应前后溶液的体积变化忽略不计).在溶液M中逐滴缓慢滴加1mol/L盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
标准状况下,向100mLNaOH溶液中缓慢通入一定量的CO2气体,充分反应后,测得最后所得溶液显碱性(反应前后溶液的体积变化忽略不计).在溶液M中逐滴缓慢滴加1mol/L盐酸,所得气体的体积与所加盐酸的体积关系如图所示: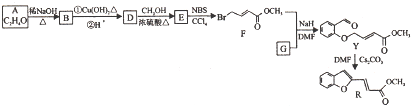
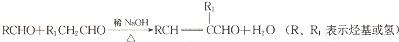
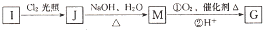
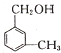 互为同系物.
互为同系物.
 已知A、B、C、D四种短周期元素,它们的核电荷数依次增大.A原子、C原子的I,能层中,都有两个未成对的电子,C、D同主族.E、F都是第四周期元素,E原子核外有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满.根据以上信息回答:
已知A、B、C、D四种短周期元素,它们的核电荷数依次增大.A原子、C原子的I,能层中,都有两个未成对的电子,C、D同主族.E、F都是第四周期元素,E原子核外有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满.根据以上信息回答: