题目内容
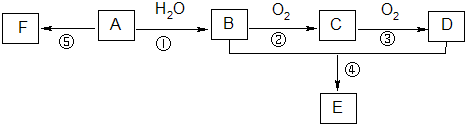
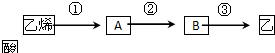
已知:A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;它有如图所示的转化关系.E是有香味的有机物,F是高分子化合物.回答下列问题:
(1)写出A的电子式 、结构简式 、空间构型 .
(2)B、D分子中的官能团名称分别是 、 .
(3)写出下列反应的化学方程式及反应类型:① ;反应类型 .② ;反应类型 .⑤ ;反应类型 .
(4)请简要写出B、F在生活中的用途:B 、F .

(1)写出A的电子式
(2)B、D分子中的官能团名称分别是
(3)写出下列反应的化学方程式及反应类型:①
(4)请简要写出B、F在生活中的用途:B
考点:有机物的推断
专题:有机物的化学性质及推断
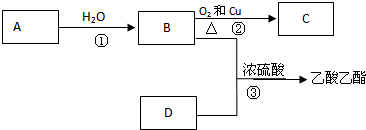
分析:A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平,则A为CH2=CH2,乙烯与水发生加成反应生成B为CH3CH2OH,乙醇发生催化氧化生成C为CH3CHO,乙醛进一步发生氧化反应生成D为CH3COOH,乙酸与乙醇分子酯化反应生成E为CH3COOCH2CH3,乙烯发生加聚反应生成高聚物F为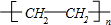 ,据此解答.
,据此解答.
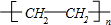 ,据此解答.
,据此解答.解答:
解:A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平,则A为CH2=CH2,乙烯与水发生加成反应生成B为CH3CH2OH,乙醇发生催化氧化生成C为CH3CHO,乙醛进一步发生氧化反应生成D为CH3COOH,乙酸与乙醇分子酯化反应生成E为CH3COOCH2CH3,乙烯发生加聚反应生成高聚物F为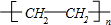 ,
,
(1)A为CH2=CH2,电子式为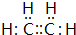 ,空间结构为:平面形,
,空间结构为:平面形,
故答案为: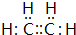 ;CH2=CH2;平面形;
;CH2=CH2;平面形;
(2)B为CH3CH2OH,含有官能团为羟基,D为CH3COOH,分子中的官能团是羧基,故答案为:羟基;羧基;
(3)反应①乙烯和水发生加成反应得到乙醇,化学方程式为:CH2=CH2+H2O
CH3CH2OH,
反应②是乙醇发生氧化反应生成乙醛,反应方程式为:2CH3CH2OH+O2
2CH3CHO+2H2O,
反应⑤是乙烯发生加聚反应生成聚乙烯,反应化学方程式为: ,
,
故答案为:CH2=CH2+H2O
CH3CH2OH,加成反应;
2CH3CH2OH+O2
2CH3CHO+2H2O,氧化反应;
 ,加聚反应;
,加聚反应;
(4)B为乙醇,75%的酒精可以用于杀菌消毒,F为聚乙烯,可以用于制造多种包装材料,故答案为:杀菌消毒;制造包装材料.
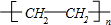 ,
,(1)A为CH2=CH2,电子式为
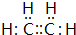 ,空间结构为:平面形,
,空间结构为:平面形,故答案为:
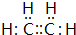 ;CH2=CH2;平面形;
;CH2=CH2;平面形;(2)B为CH3CH2OH,含有官能团为羟基,D为CH3COOH,分子中的官能团是羧基,故答案为:羟基;羧基;
(3)反应①乙烯和水发生加成反应得到乙醇,化学方程式为:CH2=CH2+H2O
| 催化剂 |
反应②是乙醇发生氧化反应生成乙醛,反应方程式为:2CH3CH2OH+O2
| Cu |
| △ |
反应⑤是乙烯发生加聚反应生成聚乙烯,反应化学方程式为:
 ,
,故答案为:CH2=CH2+H2O
| 催化剂 |
2CH3CH2OH+O2
| Cu |
| △ |
 ,加聚反应;
,加聚反应;(4)B为乙醇,75%的酒精可以用于杀菌消毒,F为聚乙烯,可以用于制造多种包装材料,故答案为:杀菌消毒;制造包装材料.
点评:本题考查有机物的推断,涉及烯、醇、羧酸等性质与转化,难度不大,是对有机基础知识的综合运用,注意对基础知识的理解掌握.

练习册系列答案
相关题目
本地的自来水是采用氯气消毒的,为了检验Cl-的存在,最好选用下列物质中( )
| A、石蕊溶液 |
| B、四氯化碳 |
| C、氢氧化钠溶液 |
| D、硝酸酸化的硝酸银溶液 |
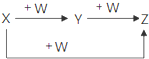 X、Y、Z、W有如图所示的转化关系,则X、W可能是( )
X、Y、Z、W有如图所示的转化关系,则X、W可能是( )①AlCl3、NaOH ②C、O2 ③Cl2、Fe ④S、O2.
| A、①②③ | B、①② |
| C、③④ | D、①②③④ |
金属镍有广泛的用途,粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述中正确的是(已知氧化性:Fe2+<Ni2+<Cu2+)( )
| A、阳极发生还原反应,其电极反应式:Ni2++2e-═Ni |
| B、电解过程中,阳极质量的减少与阴极质量的增加相等 |
| C、电解后,溶液中存在的离子只有Fe2+ 和Zn2+ |
| D、电解后,Cu和Pt沉降在电解槽底部形成阳极泥 |
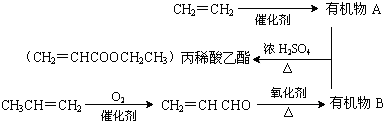
 )对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业.乙酸苯甲酯的合成路线如图:
)对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业.乙酸苯甲酯的合成路线如图: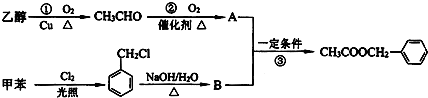
 )互为同系物的是
)互为同系物的是 B.
B.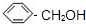 C.
C.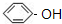 D.
D.
 C.2CH3CHO+H2
C.2CH3CHO+H2