题目内容
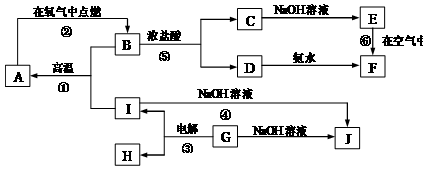
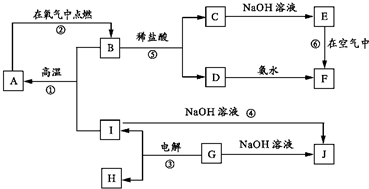 A-I分别表示中学化学中的常见物质,它们之间的相互转化关系如下图所示(部分反应物、生成物没有列出),且已知G是一种两性氧化物,A、B、C、D、E、F六种物质中均含有同一种元素,F为红褐色沉淀.
A-I分别表示中学化学中的常见物质,它们之间的相互转化关系如下图所示(部分反应物、生成物没有列出),且已知G是一种两性氧化物,A、B、C、D、E、F六种物质中均含有同一种元素,F为红褐色沉淀.请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素是
Fe
Fe
(写元素符号).(2)写出物质C、G的化学式:C
FeCl2
FeCl2
,GAl2O3
Al2O3
.(3)写出反应①、⑥的化学方程式:
反应①:
8Al+3Fe3O4
9Fe+4Al2O3
| ||
8Al+3Fe3O4
9Fe+4Al2O3
.反应⑥:
| ||
4Fe(OH)2+O2+2H2O=4Fe(OH)3
4Fe(OH)2+O2+2H2O=4Fe(OH)3
.分析:G是一种两性氧化物,应为Al2O3,与NaOH反应生成NaAlO2,则J为NaAlO2,电解生成O2和Al,由反应④可知,I为Al,则H为O2,F为红褐色沉淀,则应为Fe(OH)3,则D为FeCl3,E为Fe(OH)2,C为FeCl2,所以B为Fe3O4,与Al在高温下发生铝热反应生成A,A为Fe,根据物质的性质可进一步书写有关反应的化学方程式.
解答:解:(1)G是一种两性氧化物,应为Al2O3,与NaOH反应生成NaAlO2,则J为NaAlO2,电解生成O2和Al,由反应④可知,I为Al,则H为O2,F为红褐色沉淀,则应为Fe(OH)3,则D为FeCl3,E为Fe(OH)2,C为FeCl2,所以B为Fe3O4,与Al在高温下发生铝热反应生成A,A为Fe,所以A、B、C、D、E、F六种物质中所含的同一种元素是Fe,故答案为:Fe;
(2)由(1)分析可知,C为FeCl2,G为Al2O3,故答案为:FeCl2;Al2O3;
(3)反应①Fe3O4为与Al在高温下发生铝热反应生成Fe,反应的方程式为8Al+3Fe3O4
9Fe+4Al2O3,反应⑥为具有还原性的Fe(OH)2与空气中的氧气反应生成Fe(OH)3,反应的方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:8Al+3Fe3O4
9Fe+4Al2O3;4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(2)由(1)分析可知,C为FeCl2,G为Al2O3,故答案为:FeCl2;Al2O3;
(3)反应①Fe3O4为与Al在高温下发生铝热反应生成Fe,反应的方程式为8Al+3Fe3O4
| ||
故答案为:8Al+3Fe3O4
| ||
点评:本题考查无机物的推断,题目难度中等,本题注意根据物质的性质和典型反应现象用逆推的方法,正确推断物质的种类是解答该题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目


 _________________
_________________