题目内容
9.在密闭容器中发生反应X(g)+3Y(g)?2Z(g),若X Y Z的起始浓度分别为0.1mol/L 0.3mol/L 0.2mol/L,则平衡时各物质的浓度可能是( )| A. | X为0.2 mol/L | B. | Y为0.1 mol/L | ||
| C. | Z为0.4 mol/L | D. | Z为0.1 mol/L时,Y为0.4mol/L |
分析 化学平衡的建立,既可以从正反应开始,也可以从逆反应开始,或者从正逆反应开始,不论从哪个方向开始,物质都不能完全反应,利用极限法假设完全反应,计算出相应物质的浓度变化量,实际变化量小于极限值,据此判断分析.
解答 解:若反应向正反应进行,假定完全反应,则:
X(g)+3Y(g)?2Z(g)
开始(mol/L):0.1 0.3 0.2
变化(mol/L):0.1 0.3 0.2
平衡(mol/L):0 0 0.4
若反应逆反应进行,假定完全反应,则:
X(g)+3Y(g)?2Z(g)
开始(mol/L):0.1 0.3 0.2
变化(mol/L):0.1 0.3 0.2
平衡(mol/L):0.2 0.6 0
由于为可逆反应,物质不能完全转化所以平衡时浓度范围为0<c(X)<0.2,0<c(Y)<0.6,0<c(Z)<0.4,故B正确、ACD错误;
故选:B.
点评 本题考查化学平衡的建立,关键是利用可逆反应的不完全性,运用极限假设法解答,难度不大.

练习册系列答案
相关题目
20.下列关于Na2CO3和NaHCO3的说法中,不正确的是( )
| A. | 均溶于水 | B. | 均为白色固体 | ||
| C. | 受热均易分解 | D. | 其水溶液均能使酚酞溶液变红 |
14.下列有关海水综合利用的说法正确的是( )
| A. | 从海水中可以得到NaCl,电解熔融NaCl可获得Cl2 | |
| B. | 海水中含有钾元素,只需经过物理变化就可以得到钾单质 | |
| C. | 海水蒸发制海盐的过程只发生了化学变化 | |
| D. | 利用电解的方法可以从海水中获取淡水 |
1.将一定质量的铁片,投入盛有1L 0.9mol/L CuSO4溶液的烧杯里,一段时间后取出铁片,洗净、烘干、称量,质量增加了0.64g,若反应后溶液的体积没有变化,则反应后溶液中Cu2+的浓度为( )
| A. | 0.89mol/L | B. | 0.82mol/L | C. | 0.78mol/L | D. | 0.60mol/L |
18.下列关于油脂的叙述中,不正确的是( )
| A. | 油脂没有固定的熔点和沸点,油脂是混合物 | |
| B. | 天然油脂大多是由混甘油酯分子构成的混合物 | |
| C. | 油脂的主要成分是高级脂肪酸的甘油酯,是酯的一种 | |
| D. | 从溴水中提取溴可用植物油作萃取剂 |
19.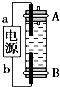 某同学设计了一种利用电解法制取Fe(OH)2的实验装置(如图),通电后,溶液中产生白色沉淀,且较长时间不变色.下列说法中正确的是( )
某同学设计了一种利用电解法制取Fe(OH)2的实验装置(如图),通电后,溶液中产生白色沉淀,且较长时间不变色.下列说法中正确的是( )
 某同学设计了一种利用电解法制取Fe(OH)2的实验装置(如图),通电后,溶液中产生白色沉淀,且较长时间不变色.下列说法中正确的是( )
某同学设计了一种利用电解法制取Fe(OH)2的实验装置(如图),通电后,溶液中产生白色沉淀,且较长时间不变色.下列说法中正确的是( )| A. | 电源中a一定为负极,b一定为正极 | |
| B. | 可以用NaCl作为电解质,但不能用Na2SO4 | |
| C. | A、B两端都必须用铁作电极 | |
| D. | 阴极上发生的反应是:2H++2e-═H2↑ |
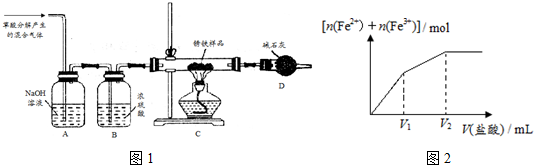
 某兴趣小组设计出如图装置(气密性已检查),验证铜与稀硝酸反应的产物,已知:FeSO4+NO═[Fe(NO)]SO4,该反应较缓慢,待生成一定量[Fe(NO)]2+时突显明显棕色.
某兴趣小组设计出如图装置(气密性已检查),验证铜与稀硝酸反应的产物,已知:FeSO4+NO═[Fe(NO)]SO4,该反应较缓慢,待生成一定量[Fe(NO)]2+时突显明显棕色.