题目内容
15.下列反应中,不属于氧化还原反应的是( )| A. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | B. | IBr+H2O═HIO+HBr | ||
| C. | 2Na2O2+4HCl═4NaCl+O2+2H2O | D. | NaH+H2O═NaOH+H2 |
分析 氧化还原反应的实质为电子的转移,特征为化合价升降,则反应中存在化合价变化的反应为氧化还原反应,没有化合价变化的反应为非氧化还原反应,据此进行解答.
解答 解:A.2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑为分解反应,反应中Mn、O元素化合价发生变化,属于氧化还原反应,故A不选;
B.反应IBr+H2O═HIO+HBr中不存在化合价变化,不属于氧化还原反应,故B选;
C.2Na2O2+4HCl═4NaCl+O2+2H2O中存在O元素化合价变化,属于氧化还原反应,故C不选;
D.NaH+H2O═NaOH+H2中存在H元素的化合价变化,属于氧化还原反应,故D不选;
故选B.
点评 本题考查了氧化还原反应的判断,题目难度不大,明确氧化还原反应的实质、特征为解答关键,注意掌握常见反应类型与氧化还原反应的关系,试题有利于提高学生的灵活应用能力.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目
6.化学反应常伴随着颜色变化,下列现象描述不正确的是( )
| A. | 无色一氧化氮气体与空气接触变为红棕色 | |
| B. | 湿润的淀粉碘化钾试纸遇氯气变蓝色 | |
| C. | 向硫酸铜溶液中滴加氢氧化钠溶液,出现白色沉淀 | |
| D. | 将足量二氧化硫气体通入品红溶液,红色逐渐褪去 |
10.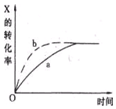 下图曲线a表示放热反应X(g)+Y(g)?Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系,若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
下图曲线a表示放热反应X(g)+Y(g)?Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系,若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
 下图曲线a表示放热反应X(g)+Y(g)?Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系,若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
下图曲线a表示放热反应X(g)+Y(g)?Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系,若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )| A. | 减压 | B. | 加大X的投入量 | C. | 升高温度 | D. | 减小体积 |
20.下列化学反应先后顺序判断正确的是( )
| A. | 向含有等物质的量的Ba(OH)2、KOH的混合溶液中通入CO2,与CO2反应的物质依次是:KOH、Ba(OH)2、BaCO3 | |
| B. | 向含有等物质的量的Fe2+、Ag+、Cu2+的混合溶液中加入Zn,与Zn反应的离子依次是:Ag+、Cu2+、Fe2+ | |
| C. | 向含有等物质的量的AlO2-、OH-、CO32-的混合溶液中滴加盐酸,与盐酸反应的物质依次是:AlO2-、Al(OH)3、OH-、CO32- | |
| D. | 在含有等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气,与氯气反应的离子依次是:I-、Br-、Fe2+ |
7. (一)(1)化学式为C6Hm的烷烃,m值等于14;请写出HCl的电子式
(一)(1)化学式为C6Hm的烷烃,m值等于14;请写出HCl的电子式 .
.
(二)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图.
(2)请写出N2和H2反应的热化学方程式:N2(g)+3H2(g)=2NH3(g)△H=-92.2KJ/mol;
(3)若已知下列数据:
试根据表中及图中数据计算N-H的键能390kJ•mol-1
(4)合成氨反应通常用铁触媒作催化剂.使用铁触媒后E1变化是:E1减小 (填“增大”、“减小、”“不变”).
(5)用NH3催化还原NOX还可以消除氮氧化物的污染.例如
4NH3(g)+3O2(g)?2N2(g)+6H2O(g)△H1=akJ•mol-1
N2(g)+O2(g)?2NO(g)△H2=b kJ•mol-1
若1mol NH3还原NO至N2,则该反应过程中的反应热△H3=$\frac{a-3b}{4}$kJ/mol(用含a、b的式子表示)
 (一)(1)化学式为C6Hm的烷烃,m值等于14;请写出HCl的电子式
(一)(1)化学式为C6Hm的烷烃,m值等于14;请写出HCl的电子式 .
.(二)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图.
(2)请写出N2和H2反应的热化学方程式:N2(g)+3H2(g)=2NH3(g)△H=-92.2KJ/mol;
(3)若已知下列数据:
| 化学键 | H-H | N≡N |
| 键能/kJ•mol-1 | 435 | 943 |
(4)合成氨反应通常用铁触媒作催化剂.使用铁触媒后E1变化是:E1减小 (填“增大”、“减小、”“不变”).
(5)用NH3催化还原NOX还可以消除氮氧化物的污染.例如
4NH3(g)+3O2(g)?2N2(g)+6H2O(g)△H1=akJ•mol-1
N2(g)+O2(g)?2NO(g)△H2=b kJ•mol-1
若1mol NH3还原NO至N2,则该反应过程中的反应热△H3=$\frac{a-3b}{4}$kJ/mol(用含a、b的式子表示)
4.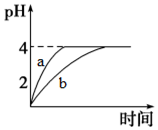 电离平衡、水解平衡、沉淀溶解平衡是溶液中的三大平衡.请回答下列问题:
电离平衡、水解平衡、沉淀溶解平衡是溶液中的三大平衡.请回答下列问题:
(1)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示.则图中表示醋酸溶液中pH变化曲线的是b(填“a”或“b”).设盐酸中参加反应的Zn粒质量为m1,醋酸溶液中参加反应的Zn粒质量为m2,则m1<m2(选填“<”、“=”或“>”).
(2)25℃时,向水的电离平衡体系中加入适量碳酸钠固体,其水解方程式为CO32-+H2O?HCO3-+OH-、HCO3-+H2O?H2CO3+OH-,测得溶液的pH=12,则由水电离出的c(OH-)=0.01mol•L-1.
(3)生活中常用用醋酸除去水垢(主要成分CaCO3),请从平衡角度解释原因:碳酸钙存在沉淀溶解平衡,CaCO3(s)?Ca2+(aq)+CO32-(aq),醋酸为弱酸存在电离平衡,CH3COOH?CH3COO-+H+,氢离子结合碳酸根离子促进程度溶解平衡正向进行,碳酸钙溶解.
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量.已知:
①在常温下,相同物质的量浓度的a.NaCN溶液 b.Na2CO3溶液c.CH3COONa溶液三种溶液的pH由小到大的顺序为c<a<b(用序号回答).
②向NaCN溶液中通入少量的CO2,发生反应的离子方程式为CO2+H2O+CN-=HCO3-+HCN.
③25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=9.9×10-7 mol•L-1(填精确值).
 电离平衡、水解平衡、沉淀溶解平衡是溶液中的三大平衡.请回答下列问题:
电离平衡、水解平衡、沉淀溶解平衡是溶液中的三大平衡.请回答下列问题:(1)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示.则图中表示醋酸溶液中pH变化曲线的是b(填“a”或“b”).设盐酸中参加反应的Zn粒质量为m1,醋酸溶液中参加反应的Zn粒质量为m2,则m1<m2(选填“<”、“=”或“>”).
(2)25℃时,向水的电离平衡体系中加入适量碳酸钠固体,其水解方程式为CO32-+H2O?HCO3-+OH-、HCO3-+H2O?H2CO3+OH-,测得溶液的pH=12,则由水电离出的c(OH-)=0.01mol•L-1.
(3)生活中常用用醋酸除去水垢(主要成分CaCO3),请从平衡角度解释原因:碳酸钙存在沉淀溶解平衡,CaCO3(s)?Ca2+(aq)+CO32-(aq),醋酸为弱酸存在电离平衡,CH3COOH?CH3COO-+H+,氢离子结合碳酸根离子促进程度溶解平衡正向进行,碳酸钙溶解.
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量.已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
②向NaCN溶液中通入少量的CO2,发生反应的离子方程式为CO2+H2O+CN-=HCO3-+HCN.
③25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=9.9×10-7 mol•L-1(填精确值).
5.下列离子方程式正确的是( )
| A. | 过氧化钠投入到水中:2Na2O2+2H2O=4Na++4OH-+O2↑ | |
| B. | 氯化铵溶液与浓NaOH 溶液加热:NH4++OH-=NH3•H2O | |
| C. | 氯化铝溶液中滴入过量氨水:Al3++3NH3•H2O=Al(OH)3↓+3 NH4+ | |
| D. | 实验室制取氯气:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$ Mn2++Cl2↑+2Cl-+2H2O |
 判断如图装置的名称:B池为电解池(填“原电池”或“电解池”)当C2极析出224mL气体(标准状况)时:锌的质量减少(填“增加”或“减少”).
判断如图装置的名称:B池为电解池(填“原电池”或“电解池”)当C2极析出224mL气体(标准状况)时:锌的质量减少(填“增加”或“减少”).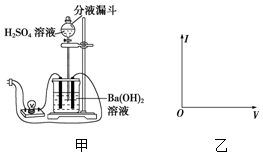 使用中学常用的实验器材,设计一个实验观察Ba(OH)2与H2SO4在溶液中的反应导电性的变化,并回答问题:
使用中学常用的实验器材,设计一个实验观察Ba(OH)2与H2SO4在溶液中的反应导电性的变化,并回答问题: