题目内容
配制250mL 1.0mol?L-1H2SO4溶液,需用98%的浓硫酸溶液(ρ=1.84g/cm3)体积为多少?取25mL 1.0mol?L-1H2SO4溶液与足量的锌反应,在标准状况下产生多少升H2?求硫酸锌的物质的量?
考点:物质的量浓度的相关计算,化学方程式的有关计算
专题:计算题
分析:根据c=
计算98%的浓硫酸溶液的物质的量浓度,再利用稀释定律计算需要浓硫酸的体积;
根据氢元素守恒可知n(H2)=n(H2SO4),再根据V=nVm计算氢气的体积.n(ZnSO4)=n(H2).
| 1000ρω |
| M |
根据氢元素守恒可知n(H2)=n(H2SO4),再根据V=nVm计算氢气的体积.n(ZnSO4)=n(H2).
解答:
解:质量分数98%,密度1.84g/mL的浓硫酸溶液的物质的量浓度为
mol/L=18.4mol/L,令配制250mL1.0mol/LH2SO4溶液,需用98%的浓硫酸体积为V,根据稀释定律,稀释前后溶质的物质的量不变,则18.4mol/L×V=250mL×1.0mol/L,解得V=13.59mL.
根据氢元素守恒可知n(H2)=n(H2SO4)=0.025L×1.0mol/L=0.025mol,标准状况下H2体积为0.025mol×22.4L/mol=0.56L;
n(ZnSO4)=n(H2)=0.025mol.
答:需用98%的浓硫酸溶液体积为13.59mL;
标准状况下生成H2体积为0.56L;
硫酸锌的物质的量为0.025mol.
| 1000×1.84×98% |
| 98 |
根据氢元素守恒可知n(H2)=n(H2SO4)=0.025L×1.0mol/L=0.025mol,标准状况下H2体积为0.025mol×22.4L/mol=0.56L;
n(ZnSO4)=n(H2)=0.025mol.
答:需用98%的浓硫酸溶液体积为13.59mL;
标准状况下生成H2体积为0.56L;
硫酸锌的物质的量为0.025mol.
点评:考查物质的量浓度与质量分数的关系、溶液配制、根据方程式的计算等,难度中等,注意基础知识的理解与掌握.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、18g NH4+ 所含原子数为4NA |
| B、10g氖气所含原子数约为6.02×1023 |
| C、标准状况下,22.4L H2O所含的分子数为NA |
| D、常温常压下,32g O2和O3的混合气体所含原子数为2NA |
一种从植物中提取的天然化合物α-damasconc,可用于制作“香水”,其结构为: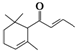 分子式为C13H20O,有关该化合物的下列说法正确的是( )
分子式为C13H20O,有关该化合物的下列说法正确的是( )
 分子式为C13H20O,有关该化合物的下列说法正确的是( )
分子式为C13H20O,有关该化合物的下列说法正确的是( )| A、一定条件下1mol该化合物最多可与2mol氢气加成 |
| B、该化合物可发生银镜反应 |
| C、1mol该化合物完全燃烧消耗19mol O2 |
| D、该化合物可发生加聚反应 |
 某环烷烃的结构像红十字会的会徽,因此有人称它为“红十字烷”结构如图,其分子式为
某环烷烃的结构像红十字会的会徽,因此有人称它为“红十字烷”结构如图,其分子式为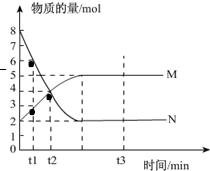 I、一定温度下,在容积为V L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示:
I、一定温度下,在容积为V L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示: