题目内容
9. 根据如图所示的装置,完成下列各空.
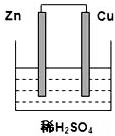
根据如图所示的装置,完成下列各空.(1)该装置中的能量转化形式是化学能转化为电能.
(2)溶液中的H+移向Cu片(填“Cu片”或“Zn片”)
(3)Zn电极的反应式为Zn-2e-=Zn2+,发生氧化反应,(填“氧化”或“还原”)
(4)Cu片为原电池的正极,现象为Cu片表面有气体放出.
分析 (1)原电池装置中化学能转化为电能;
(2)原电池工作时,阳离子向正极移动;
(3)锌为负极失电子发生氧化反应;
(4)Cu为正极,正极上溶液中的氢离子得电子生成氢气.
解答 解:该装置为原电池,活泼性强的金属锌为负极,活泼性弱的为正极;
(1)该装置为原电池,原电池装置中化学能转化为电能;故答案为:化学能;电能;
(2)原电池工作时,阳离子向正极移动,Cu为正极,则H+移向Cu片,故答案为:Cu片;
(3)锌为负极失电子发生氧化反应,则负极的电极反应为:Zn-2e-=Zn2+,故答案为:Zn-2e-=Zn2+;氧化;
(4)Cu为正极,正极上溶液中的氢离子得电子生成氢气,所以Cu片表面有气体放出,故答案为:正;Cu片表面有气体放出.
点评 本题考查学生原电池的工作原理,题目难度不大,侧重于原电池中电极的判断和电极方程式的书写的考查,注意把握溶液中离子的移动方向.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.下列装置是在制备氨气过程中所用到的装置,正确的是( )
| A. | 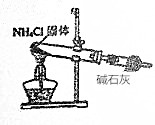 | B. |  | ||
| C. | 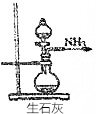 | D. |  |
17.下列物质中,只含离子键的是( )
| A. | HCl | B. | CO2 | C. | MgCl2 | D. | KOH |
14.下列反应中生成物的总能量高于反应物的总能量的是( )
| A. | CO燃烧 | B. | H2SO4与NaOH反应 | ||
| C. | Ba(OH)2•8H2O晶体和NH4Cl晶体反应 | D. | 生石灰与水作用 |
1.哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖.现向一密闭容器中充入1molN2和3molH2,在一定条件下使该反应发生.下列有关说法正确的是( )
| A. | 达到化学平衡时,N2将完全转化为NH3 | |
| B. | 达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等 | |
| C. | 达到化学平衡时,正反应和逆反应的速率都为零 | |
| D. | 达到化学平衡时,3v(N2)正=v(H2)逆 |
19.下列广告用语从化学的观点来看,不科学的是( )
| A. | 此纯净水绝对纯净,不含任何化学物质 | |
| B. | 食用油富含维生素E、油酸、亚油酸,有益于健康 | |
| C. | 八宝粥不含任何糖类物质,请糖尿病患者放心食用 | |
| D. | 低钠盐,为您的健康着想 |
 和
和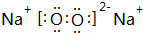 ;
; ;
;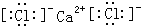 .
.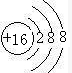 ;D与E能形成一种类似与CO2的三原子分子,且每个原子均达到了8电子稳定结构,该分子的结构式为S=C=S;化学键类型为极性共价键.
;D与E能形成一种类似与CO2的三原子分子,且每个原子均达到了8电子稳定结构,该分子的结构式为S=C=S;化学键类型为极性共价键.