题目内容
1.有机物 有多种同分异构体,其中属于酯类且含有苯环结构的共有( )
有多种同分异构体,其中属于酯类且含有苯环结构的共有( )| A. | 7种 | B. | 6种 | C. | 5种 | D. | 4种 |
分析 据有机物属于酯类,且分子结构中有苯环,则应含有-COOC-、-C6H4-(为苯环)的结构,则取代基分别为-CH3和-OOCH(存在邻间对三种),-CH2OOCH或-O0CCH3或-COOCH3,据此回答.
解答 解:由题目要求可知该有机物的同分异构体中应具有-COOC-、-C6H4-(为苯环)的结构,和苯环相连的取代基可以是-CH3和-OOCH,存在邻位取代、间位取代、对位取代三种,-CH2OOCH或-O0CCH3或-COOCH3,共六种.
故选B.
点评 本题考查限制条件下同分异构体的书写,掌握有机物的官能团和结构为解答该题的关键,难度不大,侧重于考查学生的分析能力.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
10.钠及其化合物具有广泛的用途.
(1)常温下,浓度均为0.1mol/L的下列五种钠盐溶液的pH如表;
上述盐溶液中的阴离子,结合氢离子能力最强的是CO32-;根据表中数据,浓度均为0.01mol/L的下列四种酸的溶液分别稀释100倍,pH变化最大的是C(填序号).
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)有①100mL0.1mol/L碳酸氢钠 ②100mL0.1mol/L碳酸钠两种溶液,溶液中水电离出的氢离子个数:①<②(填“>”“=”“<”下同);溶液中阴离子的物质的量浓度之和:①<②.
(3)实验室中常用氢氧化钠来进行洗气和提纯.
①当150mL1mol/L的氢氧化钠溶液吸收标况下2.24L二氧化碳时,所得溶液中各离子浓度由大到小的顺序为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有.
②几种离子开始沉淀时的pH如表:
当向含相同浓度Cu2+、Mg2+、Fe2+的溶液中滴加氢氧化钠溶液时,Cu2+(填离子符号)先沉淀,Ksp[Fe(OH)3]<Ksp[Mg(OH)2](填“>”“=”或“<”),要使0.2mol/L硫酸铜溶液中铜离子沉淀较为完全(使铜离子浓度降至原来的千分之一),则应向溶液里加入氢氧化钠溶液使溶液pH为6.( Ksp[Cu(OH)2]=2×10-20 )
(1)常温下,浓度均为0.1mol/L的下列五种钠盐溶液的pH如表;
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)有①100mL0.1mol/L碳酸氢钠 ②100mL0.1mol/L碳酸钠两种溶液,溶液中水电离出的氢离子个数:①<②(填“>”“=”“<”下同);溶液中阴离子的物质的量浓度之和:①<②.
(3)实验室中常用氢氧化钠来进行洗气和提纯.
①当150mL1mol/L的氢氧化钠溶液吸收标况下2.24L二氧化碳时,所得溶液中各离子浓度由大到小的顺序为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有.
②几种离子开始沉淀时的pH如表:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
11.下列离子方程式书写正确的是( )
| A. | 澄清石灰水跟过量CO2气体反应:Ca(OH)2+CO2=CaCO3↓+H2O | |
| B. | 稀硫酸与Cu反应:2H++Cu=Cu2++H2↑ | |
| C. | 腐蚀法制作印刷线路板:2Fe3++Cu=2Fe2++Cu2+ | |
| D. | 铁粉加入AgNO3溶液中:Fe+Ag+=Fe2++Ag |
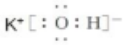 .
.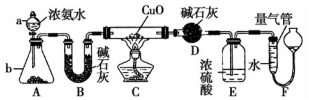 某课外活动小组欲利用CuO与NH4反应,研究NH3的某种性质并测定其组成,设计了如图实验装置(夹持装置未画出)进行实验.请回答下列问题:
某课外活动小组欲利用CuO与NH4反应,研究NH3的某种性质并测定其组成,设计了如图实验装置(夹持装置未画出)进行实验.请回答下列问题: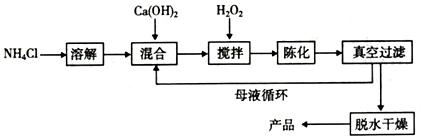
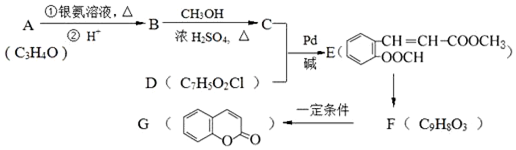

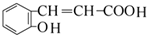 .
.
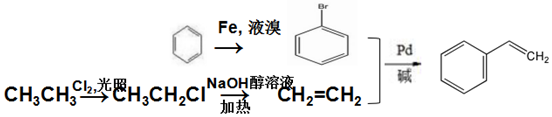 .
.