题目内容
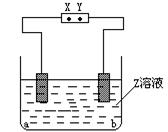
下图中X、Y分别是直流电源的两极,通电后发现a极极板质量增加,b极板处有无色无臭气体放出,符合这一情况的是

A
解析:
由“通电后发现a极板质量增加”,可知这是电解质溶液中的金属阳离子在a极板上放电,发生还原反应析出金属单质的缘故。所以a极一定是阴极,则与a极板相连接的直流电源的X极应为负极。选项C中X极为正极,故排除。
选项B中的电解液为NaOH溶液,电解时在阴极上放电的是水电离出的H+离子,在a极上析出氢气,没有金属单质析出,a极板的质量不会增加。选项B不符合题意。
选项D中的电解液为CuCl2溶液,电解时Cu2+在阴极上放电析出Cu单质,a极板的质量增加,但在阳极(b极)上是Cl-放电,b极板处有黄绿色、有刺激性臭味的氯气放出。这与题给“b极板处有无色无臭气体放出”不符合,从而排除选项D。
选项A的电解液为CuSO4溶液,电解时阴极(a极)上析出铜,使 a极板质量增加;阳极(b极)上是水电离出的OH-离子放电,析出无色无臭的气体。选项A符合题意。

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
下图中X、Y分别是直流电源的两极,通电7 s 后发现Ⅰ极板质量增加,Ⅱ极板处有无色、无臭气体放出,在这7 s内流经该装置的电子数为n mol,已知NA为阿伏加德罗常数,q为电子电荷量,符合这一情况的正确选择是

| Ⅰ极板 | Ⅱ极板 | X电极 | 装置中电流 | W溶液 |
A | 石墨 | 石墨 | 正极 |
| AgNO3 |
B | Cu | 石墨 | 负极 |
| CuCl2 |
C | Zn | 石墨 | 负极 |
| CuSO4 |
D | 石墨 | 石墨 | 负极 |
| CuSO4 |
下图中x、y分别是直流电源的两极,通电后发现a极板质量增加,b极板有无色无臭气体放出,符合这一情况的是( )

图4-5
| a极板 | b极板 | x电极 | 溶质 |
A | 锌 | 石墨 | 负极 | CuSO4 |
B | 石墨 | 石墨 | 负极 | NaOH |
C | 银 | 铁 | 正极 | AgNO3 |
D | 铜 | 石墨 | 负极 | CuCl2 |

