题目内容
根据下表中部分短周期元素的原子半径及主要化合价判断,下列叙述正确的是
|
元素代号 |
L |
M |
Q |
R |
T |
|
原子半径/nm |
0.160 |
0.143 |
0.075 |
0.102 |
0.074 |
|
主要化合价 |
+2 |
+3 |
+5、+3 |
+6、-2 |
-2 |
A. 离子半径: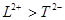
B. 氢化物的还原性:
C. M与T形成的化合物只能与盐酸反应,不与 溶液反应
溶液反应
D. 一定条件下,T的单质可将Q从其氢化物中置换出来
【答案】
D
【解析】根据元素的主要化合价和原子半径可知,L是镁,M是Al,Q是N,R是S,T是O。核外电子排布相同的微粒,其微粒半径随原子序数的增大而减小,所以A不正确,应该是 。非金属性越强,相应氢化物的还原性越弱,非金属性是O大于S,所以选项B不正确。C不正确,该化合物是氧化铝,属于两性氧化物,也能和氢氧化钠溶液反应。所以正确的答案选D。
。非金属性越强,相应氢化物的还原性越弱,非金属性是O大于S,所以选项B不正确。C不正确,该化合物是氧化铝,属于两性氧化物,也能和氢氧化钠溶液反应。所以正确的答案选D。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
根据下表中部分短周期元素的原子半径及主要化合价判断,下列叙述正确的是( )
|
根据下表中部分短周期元素的原子半径及主要化合价信息,
|
根据下表中部分短周期元素的原子半径及主要化合价判断,下列叙述正确的是( )
A.离子半径:L2+>T2-
B.氢化物的还原性:H2T>H2R
C.M与T形成的化合物只能与盐酸反应,不与NaOH溶液反应
D.一定条件下,T的单质可将Q从其氢化物中置换出来
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.075 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +5、+3 | +6、-2 | -2 |
A.离子半径:L2+>T2-
B.氢化物的还原性:H2T>H2R
C.M与T形成的化合物只能与盐酸反应,不与NaOH溶液反应
D.一定条件下,T的单质可将Q从其氢化物中置换出来