题目内容
4.在反应3Cl2+8NH3=N2+6NH4Cl中,氧化剂与还原剂分子个数之比为( )| A. | 8:3 | B. | 3:8 | C. | 3:2 | D. | 1:3 |
分析 氯气是氧化剂氨气是还原剂,氨气只有一部分作还原剂,据电子守恒计算氧化剂和还原剂的个数比.
解答 解:1mol氯气反应转移2mol电子,1mol氨气作还原剂转移3mol电子,利用最小公倍法可知,氧化剂氯气和还原剂氨气的物质的量之比为3:2,即分子个数比为3:2,故选C.
点评 本题考查了氧化还原反应中的电子守恒,注意参加反应的氨气不全是还原剂,题目难度不大.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
14.25℃时,将amol•L-1、pH=m的一元酸HX溶液与bmol•L-1、pH=n的一元碱YOH溶液等体积混合,下列说法正确的是( )
| A. | 若a=b,则混合后溶液中一定有:c(X-)=c(Y+)>c(H+)=c(OH-) | |
| B. | 若m+n=14,则混合后溶液一定显中性 | |
| C. | 若混合后溶液中c(X-)<c(Y+),则该混合溶液一定显碱性 | |
| D. | 若a=b,混合后溶液pH<7,则一定生成强酸弱碱盐 |
15.食品卫生与身体健康密切相关,下列物质可以用作食品添加剂的是( )
| A. | 三聚氰胺 | B. | 苏丹红 | C. | 工业酒精 | D. | 柠檬酸钠 |
19.下列分散系当有一束平行光通过时,会产生丁达尔效应的是( )
| A. | 氯化钠溶液 | B. | 酒精溶液 | C. | 氯水 | D. | 氢氧化铁胶体 |
9.pH=3和 PH=5的盐酸,等体积混合,混合后(假设体积不变)的PH为( )
| A. | 3 | B. | 3.1 | C. | 3.2 | D. | 3.3 |
16.下列实验可达到实验目的是( )
| A. | 可加入酸性KMnO4溶液鉴别苯、环己烯和己烷 | |
| B. | 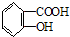 与适量NaOH溶液反应制备 与适量NaOH溶液反应制备 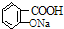 | |
| C. | 向卤代烃水解后的溶液中直接加入硝酸银溶液,可以确定卤代烃中的卤元素 | |
| D. | 利用盐析、过滤可将蛋白质和NaCl溶液分离 |
3.一定条件下,在体积为10L的恒容密闭容器中,发生如下反应:2X(g)+Y(g)?Z(g),经60s达到平衡,生成0.3mol Z,下列说法正确的是( )
| A. | 用Y 表示的化学反应速率为0.005 mol/(L•s) | |
| B. | 将容器体积变为20 L,Z的平衡浓度变为原来的$\frac{1}{2}$ | |
| C. | 若升高温度Y的转化率减小,则正反应为放热反应 | |
| D. | 达到平衡时,Y与Z的浓度相等 |
 ;N2的电子式
;N2的电子式 ;
;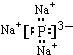 ,其中的化学键为离子键.
,其中的化学键为离子键.