题目内容
19.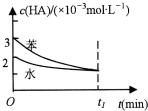 常温下,将一定量的一元有机弱酸:HA加入到100mL水与100mL苯的混合体系中,HA在水中部分电离:HA?H++A-,在苯中则部分发生双聚反应:2HA?(HA)2.在水和苯中,HA的起始浓度及平衡浓度关系如图所示.下列有关该混合体系说法正确的是( )
常温下,将一定量的一元有机弱酸:HA加入到100mL水与100mL苯的混合体系中,HA在水中部分电离:HA?H++A-,在苯中则部分发生双聚反应:2HA?(HA)2.在水和苯中,HA的起始浓度及平衡浓度关系如图所示.下列有关该混合体系说法正确的是( )| A. | HA在水中的电离速率大于其在苯中的双聚速率 | |
| B. | t1时刻在水中和苯中c(A-)相同 | |
| C. | 向上述的混合体系中加入少量水和苯的混合物,则两平衡均正移,c(HA)均减小 | |
| D. | 用10mL 0.05mol•L-1的NaOH溶液可恰好中和混合体系中的HA |
分析 A.由图象可知,在相同时间内,在苯中HA的浓度变化值大;
B.在苯中不存在A-;
C.水溶液中促进了电离,平衡向着正向移动,苯体系中平衡向着分子数增大的方向移动;
D.计算混合物中HA的物质的量,HA与NaOH等物质的量反应.
解答 解:A.由图象可知,在相同时间内,在苯中HA的浓度变化值大,所以HA在水中的电离速率小于其在苯中的双聚速率,故A错误;
B.在苯中则部分发生双聚反应:2HA?(HA)2,所以在苯中不存在A-,故B错误;
C.向上述的混合体系中加入少量水和苯的混合物,水溶液中浓度越小,电离程度越大,则上述平衡正移,且c(HA)减小;而苯溶液中稀释过程,平衡将向分子数增大方向移动,即向逆方向移动,但c(HA)会减小,故C错误;
D.10mL 0.05mol•L-1的NaOH溶液中n(NaOH)=0.0005mol,混合体系中的HA的物质的量为0.0005mol,则HA与NaOH等物质的量恰好反应,故D正确.
故选D.
点评 本题考查了弱电解质的电离,明确弱电解质的电离特点以及图象中所给的信息是解本题关键,考查学生知识迁移能力、分析能力、以及对信息的提取应用能力,题目难度中等.

练习册系列答案
 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
9.钡在氧气中燃烧时的得到一种钡的氧化物晶体,结构如图所示,有关说法正确的是( ) 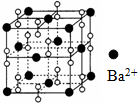

| A. | 该晶体为分子晶体 | |
| B. | 晶体的化学式为Ba2O2 | |
| C. | 该晶体晶胞结构与CsCl相似 | |
| D. | 与每个Ba2+距离相等且最近的Ba2+共有12个 |
10.已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
| A. | 质子数:c>d | B. | 氢化物的稳定性:H2Y>HZ | ||
| C. | 离子的氧化性:X+<W3+ | D. | 原子半径:X<W |
4.下列灭火剂能用于扑灭金属钠着火的是( )
| A. | 干冰灭火剂 | B. | 沙土 | C. | 干粉灭火剂 | D. | 泡沫灭火剂 |
12.在粗盐提纯的实验中,操作正确的是( )
| A. | 把浑浊的液体倒入蒸发皿中加热 | |
| B. | 开始析出晶体后用玻璃棒搅拌 | |
| C. | 待水分完全蒸干后停止加热 | |
| D. | 蒸干水分后用玻璃棒转移固体至滤纸上 |
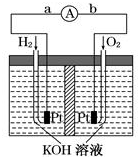 氢氧燃料电池是符合绿色化学理念的新型发电装置,图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置,图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答: 、
、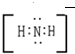 .
.