题目内容
(8分)实验室用浓盐酸和MnO2制取并探究Cl2化学性质,装置图如下图所示:
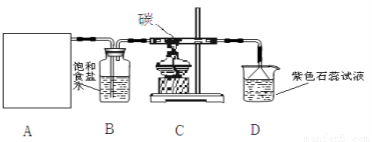
(1)A是氯气发生装置,请完成反应的离子方程式为_________________________________。除了酒精灯和导管外,还用到的玻璃仪器有_______________。
(2)从C装置出来的气体中含有CO2和HCl,写出C中反应的化学方程式_____________________。
(3)同学们在实验中发现:若用稀盐酸代替浓盐酸与MnO2混合加热没有氯气生成。“影响氯气生成的原因是什么呢?”,同学们作了如下探究:
① 提出合理假设
假设1:Cl—的浓度对反应的影响;
假设2:
(1)MnO2 + 4H+ + 2Cl- △ Mn2+ + Cl2↑+ 2H2O (2分);圆底烧瓶、分液漏斗(2分)
(2)2Cl2+2H2O+C△4HCl+CO2↑(2分) (3)① 假设2:H+的浓度对反应的影响 (2分)
【解析】
试题分析:(1)实验室制取氯气的反应中反应物为浓盐酸和二氧化锰,在加热的条件下反应生成氯气、氯化锰和水,方程式为MnO2 + 4H+ + 2Cl- △ Mn2+ + Cl2↑+ 2H2O;反应需要加热,用到酒精灯,浓盐酸盛放在分液漏斗中,二氧化锰盛放在圆底烧瓶中,还需要用到导管进行连接仪器,因此还需要的玻璃仪器是分液漏斗、圆底烧瓶;
(2)C装置中的反应物为氯气、水和碳,生成物为氯化氢和二氧化碳,根据化学方程式书写原则写出化学方程式为:2Cl2+2H2O+C△4HCl+CO2↑;
(3)稀盐酸中含有的离子是氯离子和氢离子,故猜想2为H+的浓度对反应的影响。
考点:考查氯气的实验室制法及氯气的化学性质

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案