题目内容
17.有机物A为饱和多元醇,将13.6g A在20.0L纯O2(过量)中充分燃烧并使反应后的气体依次缓缓通过浓硫酸和碱石灰后,测得气体体积分别为17.76L和6.56L(所有气体体积均在标准状况下测定).A的分子式为C5H12O4.又知A中含有2种氢原子,则A的结构简式为 .
.
分析 浓硫酸吸收水蒸气,碱石灰可以吸收二氧化碳,可知生成二氧化碳体积、剩余氧气体积,进而计算消耗氧气物质的量,设饱和多元醇的分子式为CnH2n+2Oy,燃烧方程式为:CnH2n+2Oy+$\frac{3n+1-y}{2}$O2$\frac{\underline{\;点燃\;}}{\;}$CO2+(n+1)H2O,结合生成二氧化碳、消耗氧气物质的量计算确定分子式,再结合A中含有2种氢原子确定结构简式.
解答 解:通过浓硫酸和碱石灰后气体体积仍为6.56L,为剩余的氧气,发生反应的氧气的物质的量=$\frac{20L-6.56L}{22.4L/mol}$=0.6mol,
通过浓硫酸后气体体积为17.76L,通过碱石灰后体积为6.56L,减小体积为二氧化碳体积,其物质的量为:$\frac{17.76L-6.56L}{22.4L/mol}$=0.5mol,
设饱和多元醇的分子式为CnH2n+2Oy,则:
CnH2n+2Oy+$\frac{3n+1-y}{2}$O2$\frac{\underline{\;点燃\;}}{\;}$nCO2+(n+1)H2O
(14n+16y+2)g $\frac{3n+1-y}{2}$mol nmol
13.6g 0.6mol 0.5mol
可得关系式:(14n+16y+2)g:13.6g=$\frac{3n+1-y}{2}$mol:0.6mol
$\frac{3n+1-y}{2}$mol:nmol=0.6mol:0.5mol
联立解得=5,y=4,
即A的分子式为:C5H12O4,A中含有2种氢原子,A的结构简式为: ,
,
故答案为:C5H12O4; .
.
点评 本题考查有机物分子式确定,注意利用多元饱和醇的通式进行解答,综合考查学生对知识的整合能力,难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 由NO2和N2O4组成的平衡体系加压后颜色先变深后变浅 | |
| B. | 增大压强可加快SO2转化为SO3的速率 | |
| C. | 黄绿色的氯水光照后颜色变浅 | |
| D. | 在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去 |
| X | Y | |
| Z | W | |
| T |
| A. | 氢化物稳定性Y比W强,是因为Y的氢化物中存在氢键 | |
| B. | XY2、XW2、ZY2熔沸点依次增大,都是由共价键形成的分子晶体 | |
| C. | 一定条件下,X单质能与ZY2反应生成Z单质,说明X的非金属性比Z强 | |
| D. | 根据元素周期律,可以推测T元素的单质具有半导体特性,钠能与T形成Na2T2化合物 |
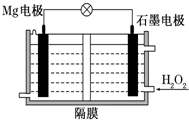 Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如下.该电池工作时,下列说法正确的是( )
Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如下.该电池工作时,下列说法正确的是( )| A. | Mg电极是该电池的正极 | B. | H2O2在石墨电极上发生氧化反应 | ||
| C. | 石墨电极附近溶液的pH增大 | D. | 电子从石墨电极移向Mg电极 |
| A. | 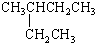 2-乙基丁烷 | B. | CH3CHBr2二溴乙烷 | ||
| C. |  2-甲基丁烯 | D. | 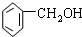 苯甲醇 |

 .
.