题目内容
2.在实验室里,某同学取一小块金属钠做钠与水反应的实验.试完成下列问题:(1)切开的金属钠暴露在空气中,最先观察到的现象是钠块表面由银白色变为暗灰色,所发生反应的化学方程式是4Na+O2═2Na2O.
(2)将钠投入水中后,钠熔化成一个小球,根据这一现象你能得出的结论是①钠与水反应放出热量,②钠的熔点低.
(3)①将一小块钠投入盛有饱和石灰水的烧杯中,不可能观察到的现象是C.
A.有气体生成 B.钠熔化成小球并在液面上游动
C.烧杯底部有银白色的金属钙生成 D.溶液变浑浊
②写出上述实验过程中反应的化学方程式为2Na+2H2O═2NaOH+H2↑.
(4)根据以上实验过程中钠所发生的有关变化,试说明金属钠保存在煤油中的目的是防止钠与空气中的氧气和水蒸气接触.
分析 (1)钠与氧气常温下反应生成氧化钠,现象钠块表面由银白色变为暗灰色;
(2)依据钠熔化成一个小球可知反应放出热量,钠的熔点低;
(3)钠投入盛有饱和石灰水,钠与水反应生成氢氧化钠和氢气,反应放热,结合氢氧化钙溶解度随着温度升高而降低及钠的物理性质解答;
(4)依据钠能够与氧气、水蒸气反应,钠的密度大于煤油解答.
解答 解:(1)钠与氧气常温下反应生成氧化钠,方程式:4Na+O2═2Na2O,现象钠块表面由银白色变为暗灰色;
故答案为:钠块表面由银白色变为暗灰色;4Na+O2═2Na2O;
(2)将钠投入水中后,钠熔化成一个小球,根据这一现象你能得出的结论是①钠与水反应放出热量,②钠的熔点低;
故答案为:钠与水反应放出热量; 钠的熔点低;
(3)①钠投入盛有饱和石灰水,钠与水反应生成氢氧化钠和氢气,反应放热,氢氧化钙溶解度随着温度升高而降低,所以看到现象为:钠熔化成小球并在液面上游动;有气泡产生;溶液变浑浊;看不到现象:烧杯底部有银白色的金属钙生成;
故选:C;
②钠与水反应生成氢氧化钠和氢气,方程式:2Na+2H2O═2NaOH+H2↑;
故答案为:2Na+2H2O═2NaOH+H2↑;
(4)钠能够与氧气、水蒸气反应,钠的密度大于煤油,钠放在煤油中能够隔绝氧气和水蒸气;
故答案为:防止钠与空气中的氧气和水蒸气接触.
点评 本题考查了元素化合物知识,侧重考查钠及钠与水的反应,明确钠的性质及钠与水反应产物是解题关键,注意氢氧化钙溶解度随着温度升高而降低特点,题目难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
13.A、B、C、D、E、F是中学化学中常见的六种短周期元素,有关位置及信息如下:A的气态氢化物能使湿润的红色石蕊试纸变蓝;C单质在实验室一般保存在煤油中;F的最高价氧化物对应的水化物既能与酸反应又能与碱反应,G单质是日常生活中用量最大的金属,易被腐蚀.请回答下列问题:
(1)G元素在周期表中的位置是第四周期第Ⅷ族.
(2)A与B可组成质量比为7:16的三原子分子,该分子与水反应的化学方程式:3NO2+H2O=2HNO3+NO;
(3)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若a=b,则所得溶液的pH<7(填“>“或“<”或“=”),若所得溶液的pH=7,则a>b(填“>“或“<”或“=”)
(4)写出F的单质与NaOH溶液反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(5)已知一定量的E单质能在B2(g)中燃烧,其可能的产物及能量关系如图1所示:请写出一定条件下EB2(g)与E(s)反应生成EB(g)的热化学方程式CO2(g)+C(s)=2CO(g)△H=+172.5kJ/mol.
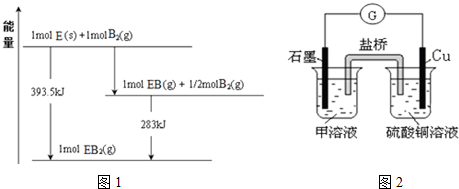
(6)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图2所示,其反应中正极反应式为Fe3++e-=Fe2+.
| … | E | A | B | ||
| C | … | D |
(2)A与B可组成质量比为7:16的三原子分子,该分子与水反应的化学方程式:3NO2+H2O=2HNO3+NO;
(3)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若a=b,则所得溶液的pH<7(填“>“或“<”或“=”),若所得溶液的pH=7,则a>b(填“>“或“<”或“=”)
(4)写出F的单质与NaOH溶液反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(5)已知一定量的E单质能在B2(g)中燃烧,其可能的产物及能量关系如图1所示:请写出一定条件下EB2(g)与E(s)反应生成EB(g)的热化学方程式CO2(g)+C(s)=2CO(g)△H=+172.5kJ/mol.

(6)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图2所示,其反应中正极反应式为Fe3++e-=Fe2+.
10.下列有关实验操作、现象和结论正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将某气体通入FeCl2溶液中 | 溶液由浅绿色变为黄色 | 该气体中一定含有Cl2 |
| B | 将某气体通入品红溶液中 | 品红溶液褪色 | 该气体中一定含有SO2 |
| C | 将某气体通过灼热的CuO粉末 | 粉末由黑变红 | 该气体中一定含有H2 |
| D | 将某气体与湿润的红色石蕊试纸接触 | 试纸变蓝色 | 该气体中一定含有NH3 |
| A. | A | B. | B | C. | C | D. | D |
17.已知C-C单键可以绕键轴旋转,结构简式为 的烃,下列说法中正确的是( )
的烃,下列说法中正确的是( )
 的烃,下列说法中正确的是( )
的烃,下列说法中正确的是( )| A. | 在 FeBr3的催化作用下可与溴水发生取代反应 | |
| B. | 该烃与足量 H2的加成产物一氯代物最多有四种 | |
| C. | 分子中至少有10个碳原子处于同一平面上 | |
| D. | 该烃是苯的同系物 |
7.在下列物质中,能够导电的电解质是( )
| A. | 食盐晶体 | B. | 无水乙醇 | C. | 熔融的氯化钾 | D. | 稀硫酸溶液 |
11.ClO2是一种消毒杀菌效率高、二次污染小的水处理剂.实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4═2ClO2↑+K2SO4+2CO2↑+2H2O下列说法正确的是( )
| A. | KClO3在反应中得到电子 | |
| B. | ClO2是氧化产物 | |
| C. | H2C2O4在反应中被氧化 | |
| D. | 1 mol KClO3参加反应,有2 mol电子转移 |