题目内容
物质A、B、C、D、E、F、G、H、I、J、K有如图转化关系,其中气体D、E为单质,试回答:

(1)写出下列物质的化学式:A是 ,D是 ,
(2)写出反应“I→J”的离子方程式: ;
(3)写出反应“F→G”的化学方程式: ;
(4)在溶液I中滴入NaOH溶液,可观察到的现象是: .

(1)写出下列物质的化学式:A是
(2)写出反应“I→J”的离子方程式:
(3)写出反应“F→G”的化学方程式:
(4)在溶液I中滴入NaOH溶液,可观察到的现象是:
考点:无机物的推断
专题:推断题
分析:黄绿色气体E为Cl2,红褐色沉淀K为Fe(OH)3,则金属H为Fe,故气体D为H2,气体B为HCl,I为FeCl2,J为FeCl3,金属A与盐酸反应生成氯化铝与氢气,则C为AlCl3,F为Al(OH)3,G为NaAlO2,据此解答.
解答:
解:黄绿色气体E为Cl2,红褐色沉淀K为Fe(OH)3,则金属H为Fe,故气体D为H2,气体B为HCl,I为FeCl2,J为FeCl3,金属A与盐酸反应生成氯化铝与氢气,则C为AlCl3,F为Al(OH)3,G为NaAlO2,
(1)由上述分析可知,A是Al,D是 H2,故答案为:Al;H2;
(2)反应“I→J”的离子方程式:2Fe2++Cl2=2Fe3++2Cl-,故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(3)反应“F→G”的化学方程式:Al(OH)3+NaOH=NaAlO2+2H2O,故答案为:Al(OH)3+NaOH=NaAlO2+2H2O;
(4)在溶液FeCl2中滴入NaOH溶液,先生成氢氧化亚铁,然后被氧化为氢氧化铁,可观察到的现象是:先出现灰白色沉淀然后变成灰绿色,最后变成红褐色,
故答案为:先出现灰白色沉淀然后变成灰绿色,最后变成红褐色.
(1)由上述分析可知,A是Al,D是 H2,故答案为:Al;H2;
(2)反应“I→J”的离子方程式:2Fe2++Cl2=2Fe3++2Cl-,故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(3)反应“F→G”的化学方程式:Al(OH)3+NaOH=NaAlO2+2H2O,故答案为:Al(OH)3+NaOH=NaAlO2+2H2O;
(4)在溶液FeCl2中滴入NaOH溶液,先生成氢氧化亚铁,然后被氧化为氢氧化铁,可观察到的现象是:先出现灰白色沉淀然后变成灰绿色,最后变成红褐色,
故答案为:先出现灰白色沉淀然后变成灰绿色,最后变成红褐色.
点评:本题考查无机物推断,物质的颜色是推断突破口,需要学生熟练掌握元素化合物性质,难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、已知某温度下纯水中的c(H+)=2×l0-7mol.L-1,据此无法求出水中c(OH-) | ||||||||||
| B、已知MgCO3的KSP=6.82×l0-6,则在含有固体MgCO3的MgCl2、Na2CO3溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)?c(CO32-)=6.82×10-6 mol2.L-2 | ||||||||||
C、常温下
| ||||||||||
D、已知:
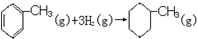 的焓变 的焓变 |
如图是某硫酸试剂瓶标签上的部分内容,据此判断下列说法不正确的是( )


| A、该硫酸的物质的量浓度为l8.4mol/L |
| B、该硫酸与等体积的水混合所得溶液的质量分数大于49% |
| C、配制200.0mL4.6mol/L的稀硫酸需取该硫酸50.0mL |
| D、6.4gCu与足量的该硫酸充分反应产生的气体一定为2.24L |
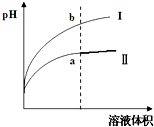
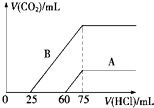 取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:
取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:
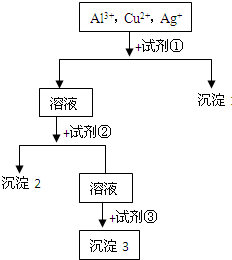 某溶液中含有Al3+,Cu2+,Ag+,现用NaOH溶液、盐酸和试剂X将这三种离子逐一沉淀分离.其流程图如图:
某溶液中含有Al3+,Cu2+,Ag+,现用NaOH溶液、盐酸和试剂X将这三种离子逐一沉淀分离.其流程图如图: