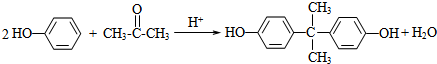题目内容
8.下列说法中正确的是( )| A. | 中和热测定实验时,如果没有环形玻璃搅拌棒,可用环形铜质搅拌棒代替 | |
| B. | 用pH试纸测定溶液的pH值时,先把试纸放在待测液中,然后比色 | |
| C. | 含NO2球放在热水中的平衡球颜色加深,放入冷水中的平衡球颜色变浅 | |
| D. | 向盛有FeCl3溶液的试管中加入KSCN溶液,立即生成血红色沉淀 |
分析 A.铜质搅拌棒的传热能力大于环形玻璃搅拌棒;
B.用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH;
C.2NO2(g)?N2O4(g)正反应放热;
D.向FeCl3溶液中加入KSCN溶液,观察到溶液呈血红色.
解答 解:A.铜质搅拌棒的传热能力大于环形玻璃搅拌棒,为了减少能量损失,不可用环形铜质搅拌棒代替环形玻璃搅拌棒,故A错误;
B.不能把试纸放在待测液中,故B错误;
C.2NO2(g)?N2O4(g)正反应放热,放在热水中的平衡球颜色加深,放入冷水中的平衡球颜色变浅,故C正确;
D.向某FeCl3溶液中加入KSCN溶液,观察到溶液呈血红色,得不到沉淀,故D错误.
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及中和热测定、pH试纸使用、化学平衡以及离子检验等,把握反应原理及反应与现象的关系为解答的关键,注意从实验的评价性及物质性质分析解答,题目难度不大.

练习册系列答案
 目标测试系列答案
目标测试系列答案
相关题目
18.有五种饱和溶液①Ba(NO3)2 ②Ca(OH)2 ③NaAlO2 ④Na2CO3 ⑤NH3和NaCl,分别持续通入CO2,最终得到沉淀或析出晶体的是( )
| A. | ①②③④⑤ | B. | ①③④⑤ | C. | ③④ | D. | ③④⑤ |
16.下列电离方程式中正确的是( )
| A. | NaHCO3═Na++H++CO32- | B. | Fe2(SO4)3═Fe3++SO42- | ||
| C. | KClO3═K++Cl-+3O2- | D. | H2SO4═2H++SO42- |
3.化学与社会、生产、生活密切相关.下列说法不正确的是( )
| A. | 家用燃气灶是化学能转化为热能的应用装置 | |
| B. | 食品放入冰箱中,因为温度低,变质速率降低,所以食品能够保存较长时间 | |
| C. | 将煤气化,有利于提供更多的能量,而且有效地减少温室气体的产生 | |
| D. | 因为食用醋中含有酸,可以用来清洗锅垢 |
13.已知:2SO2(g)+O2(g)?2SO3(g)△H=-197kJ/mol,现有容积相同的甲、乙、丙三个容器,在相同条件下分别充入的气体和反应放出的热量(Q)如下表所列:
根据以上数据,下列叙述正确的是( )
| 容器 | SO2(mol) | O2(mol) | N(mol) | Q(kJ) |
| 甲 | 2 | 1 | 0 | Q1 |
| 乙 | 1 | 0.5 | 0 | Q2 |
| 丙 | 1 | 0.5 | 1 | Q3 |
| A. | 在上述条件下反应生成1molSO3气体放热98.5 kJ | |
| B. | Q1=2Q2=2Q3=197 kJ | |
| C. | 上述条件下1mol O2参加反应放出的热量为197 kJ/mol | |
| D. | Q2<Q3<Q1<197kJ |
17.下列反应的离子方程式错误的是( )
| A. | 醋酸和足量的氢氧化钠溶液反应:H++OH-═H2O | |
| B. | 溴化亚铁溶液中通入足量的氯气:2 Fe2++4 Br-+3 Cl2═2 Fe3++2 Br2+6 Cl- | |
| C. | 用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O | |
| D. | 碳酸氢铵稀溶液中加入过量的石灰水:Ca2++HCO3-+2 OH-+NH4+═CaCO3↓+NH3•H2O+H2O |
11.下列表示氯及其化合物的化学用语正确的是( )
| A. | 中子数为20的氯原子符号:20Cl | |
| B. | HClO的结构式:H-Cl-O | |
| C. | HClO4的电离方程式:HClO4═H++ClO4- | |
| D. | Cl-的结构示意图: |
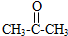 )在酸性介质中反应制得.写出反应的化学方程式
)在酸性介质中反应制得.写出反应的化学方程式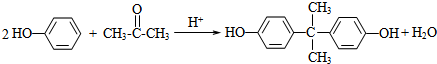
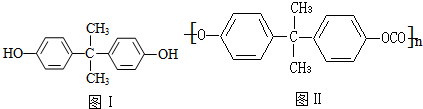
 )为原料合成一种防碎塑料--聚碳酸酯,简称PC结构简式如图Ⅱ.以PC为原料制成的婴儿奶瓶在使用过程中会析放出极少量的双酚A,长期使用可能损害婴儿的健康.
)为原料合成一种防碎塑料--聚碳酸酯,简称PC结构简式如图Ⅱ.以PC为原料制成的婴儿奶瓶在使用过程中会析放出极少量的双酚A,长期使用可能损害婴儿的健康.