题目内容
已知:P4(s、白磷)+5O2(g)═P4O10(s);△H=-2983.2kJ/mol4P(s、红磷)+5O2(g)═P4O10(s);△H=-2954kJ/mol
那么,1mol红磷转变成相应物质的量白磷时,应是( )
那么,1mol红磷转变成相应物质的量白磷时,应是( )
| A、吸收29.2kJ热量 |
| B、放出29.2kJ热量 |
| C、放出7.3kJ热量 |
| D、吸收7.3kJ热量 |
考点:有关反应热的计算
专题:化学反应中的能量变化
分析:根据盖斯定律可以计算化学反应的焓变,进而书写热化学方程式即可.
解答:
解:红磷转化为白磷的化学方程式为:4P(s、红磷)=P4(s、白磷),
可以看成是下列两个反应方程式的和:P4O10(s)=P4(s、白磷)+5O2(g);△H=2983.2kJ?mol-1;4P(s、红磷)+5O2(g)=P4O10(s);△H=-738.5×4kJ?mol-1=-2954kJ?mol-1;
根据盖斯定律,红磷转化为白磷4P(s、红磷)=P4(s、白磷)的△H=2983.2kJ/mol-2954kJ?mol-1=29.2KJ/mol,
即4P(s、红磷)=P4(s、白磷)△H=+29.2KJ/mol,红磷转化为白磷的热化学方程式可知过程是一个吸热反应,
故选A.
可以看成是下列两个反应方程式的和:P4O10(s)=P4(s、白磷)+5O2(g);△H=2983.2kJ?mol-1;4P(s、红磷)+5O2(g)=P4O10(s);△H=-738.5×4kJ?mol-1=-2954kJ?mol-1;
根据盖斯定律,红磷转化为白磷4P(s、红磷)=P4(s、白磷)的△H=2983.2kJ/mol-2954kJ?mol-1=29.2KJ/mol,
即4P(s、红磷)=P4(s、白磷)△H=+29.2KJ/mol,红磷转化为白磷的热化学方程式可知过程是一个吸热反应,
故选A.
点评:本题考查学生利用盖斯定律来计算化学反应的焓变这一知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列叙述不正确的是( )
A、 放电闪电时会发生反应: N2+O2═2NO |
B、 利用丁达尔效应证明烧杯中的分散系是胶体 |
C、 蔗糖中加入浓硫酸搅拌后变黑,因为浓硫酸有吸水性 |
D、 加热时熔化的铝不滴落,证明Al2O3的熔点比Al高 |
在两个容积相同的容器中,一个盛有NO气体,另一个盛有N2和O2的混合气体,在同温同压下,两容器内的气体一定具有相同的( )
| A、原子数 | B、密度 |
| C、质量 | D、摩尔质量 |
下列装置或操作能达到实验目的是( )
A、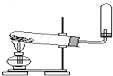 制备收集NH3 |
B、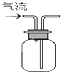 收集CO2气体 |
C、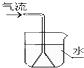 溶解吸收NH3 |
D、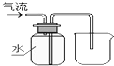 收集NO气体 |
最近,科学家冶炼出纯度高达99.999%的铝,你估计它具有性质是( )
| A、熔点比铁铝合金小 |
| B、在冷、浓HNO3中可以钝化 |
| C、在空气中放置容易生锈,进而被腐蚀 |
| D、当它与铁的粉碎粒度相同时,与4mol/L盐酸反应速率比纯铁大 |
下列实验方案能顺利达到实验目的是( )
A、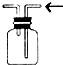 排空气法收集NO |
B、 乙醇萃取碘水中碘 |
C、 过滤 |
D、 量取9.3mL H2O |
用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A、标准状况下,5.6 L四氯化碳含有的分子数为0.25NA |
| B、标准状况下,14 g氮气含有的核外电子数为5NA |
| C、由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
| D、NA个一氧化碳分子和0.5 mol 甲烷的质量比为7:4 |