题目内容
14.写出下列反应的离子方程式.①硫酸与氢氧化钡溶液反应的离子方程式:2H++SO42-+2OH-+Ba2+=2H2O+BaSO4↓
②足量稀盐酸与碳酸氢钠溶液反应的离子方程式:H++HCO3-=H2O+CO2↑
③向足量的氢氧化钙溶液中通入二氧化碳的离子方程式:CO2+2OH-+Ca2+=2H2O+CaCO3↓
④稀硫酸清洗铁锈(Fe2O3)的离子方程式:6H++Fe2O3=3H2O+2Fe3+.
分析 ①反应生成硫酸钡和水,硫酸钡、水在离子反应中均保留化学式;
②反应生成氯化钠、水、二氧化碳;
③反应生成碳酸钙和水,碳酸钙、水、二氧化碳在离子反应中均保留化学式;
④反应生成硫酸铁、水.
解答 解:①硫酸与氢氧化钡溶液反应的离子方程式为2H++SO42-+2OH-+Ba2+=2H2O+BaSO4↓,故答案为:2H++SO42-+2OH-+Ba2+=2H2O+BaSO4↓;
②足量稀盐酸与碳酸氢钠溶液反应的离子方程式为H++HCO3-=H2O+CO2↑,故答案为:H++HCO3-=H2O+CO2↑;
③向足量的氢氧化钙溶液中通入二氧化碳的离子方程式为CO2+2OH-+Ca2+=2H2O+CaCO3↓,故答案为:CO2+2OH-+Ca2+=2H2O+CaCO3↓;
④稀硫酸清洗铁锈(Fe2O3)的离子方程式为6H++Fe2O3=3H2O+2Fe3+,故答案为:6H++Fe2O3=3H2O+2Fe3+.
点评 本题考查了离子方程式的书写,为高考的高频题,属于中等难度的试题,侧重复分解反应的离子反应考查,注意离子反应中需要保留化学式的物质,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
2.在与Al反应能放出H2的溶液中,一定能大量共存的离子组是( )
| A. | K+、Na+、HCO3-、Cl- | B. | K+、NO3-、Cl-、I- | ||
| C. | Na+、Cl-、I-、SO42- | D. | NH4+、Al3+、Cl-、SO42- |
9.下列有机物中,能发生消去反应生成2种烯烃,又能发生水解反应的是( )
| A. | 2-甲基-2-氯丙烷 | B. | 2-甲基-3-氯戊烷 | ||
| C. | 2,2-二甲基-1-氯丁烷 | D. | 1,3-二氯苯 |
19.分类是学习和研究化学的一种重要方法,下列分类合理的是( )
| A. | H2SO4和HNO3都属于酸 | B. | Na2CO3和Na2O都属于盐 | ||
| C. | NaOH 和Na2CO3都属于碱 | D. | Na2O和Na2SiO3都属于氧化物 |
6.下列混合物的分离方法不正确的是( )
| A. | 沸点不同的液体可用蒸馏的方法分离 | |
| B. | 易溶与难溶的固体混合物可用溶解、过滤、蒸发、结晶的方法分离 | |
| C. | 用酒精可以从碘水中萃取碘 | |
| D. | 汽油和水的化合物不可以用分液漏斗分离 |
3.下列溶液中Cl-的物质的量浓度与100mL 0.5mol•L-1的CuCl2溶液相同的是( )
| A. | 200 mL 0.25 mol•L-1 MgCl2溶液 | B. | 200 mL 0.25 mol•L-1 AlCl3溶液 | ||
| C. | 50 mL 1 mol•L-1 NaCl溶液 | D. | 25 mL 0.5 mol•L-1 HCl溶液 |
4.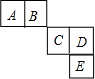 前四周期主族元素A、B、C、D、E在元素周期表中的相对位置如图所示,其中C元素原子的最外层电子数与最内层电子敦之和等于其电子总数的一半,下列说法正确的是( )
前四周期主族元素A、B、C、D、E在元素周期表中的相对位置如图所示,其中C元素原子的最外层电子数与最内层电子敦之和等于其电子总数的一半,下列说法正确的是( )
 前四周期主族元素A、B、C、D、E在元素周期表中的相对位置如图所示,其中C元素原子的最外层电子数与最内层电子敦之和等于其电子总数的一半,下列说法正确的是( )
前四周期主族元素A、B、C、D、E在元素周期表中的相对位置如图所示,其中C元素原子的最外层电子数与最内层电子敦之和等于其电子总数的一半,下列说法正确的是( )| A. | 元素A、B的所有氢化物中均只含有极性共价键 | |
| B. | 元素C、D形成的简单离子的电子总数不同 | |
| C. | 元素C、D、E形成的常见单质的熔沸点大小:E>D>C | |
| D. | C、D、E三种元素最高价氧化物对应的水化物中D的酸性最强 |
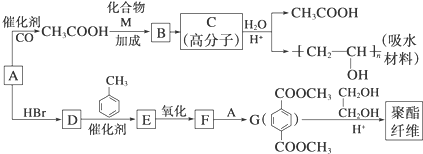
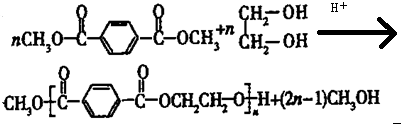 .
.