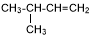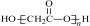题目内容
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.1 mol 甲醇中含有C-H键的数目为4NA
B.0.1mol 丙烯酸中含有双键的数目为0.1NA
C.标准状况下,11.2 L CH3CH2OH中含有的分子数目为0.5NA
D.常温常压下,7.0 g乙烯与丙烯的混合物中含有氢原子的数目为NA
D
【解析】
试题分析:1 mol 甲醇中含有C-H键的数目为3NA,故A项错误;一个丙烯酸分子中有2个双键,0.1mol 丙烯酸中含有双键的数目为0.2NA,故B项错误;CH3CH2OH 在标准状况下为液体,11.2 L CH3CH2OH的物质的量不是0.5mol,故C错误;根据极值法,7.0 g乙烯中含有氢原子的物质的量为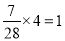 mol、7.0 g丙烯中含有氢原子的物质的量为
mol、7.0 g丙烯中含有氢原子的物质的量为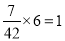 mol,故D正确。
mol,故D正确。
考点:本题考查阿伏加德罗常数。

 名校课堂系列答案
名校课堂系列答案(12分)在100 ℃时,将0.100 mol N2O4气体充入1 L恒容抽空的密闭容器中,隔一定时间对该容器内物质的浓度进行分析得到如表数据:
时间(s) | 0 | 20 | 40 | 60 | 80 |
c(N2O4)/mol·L-1 | 0.100 | c1 | 0.050 | c3 | c4 |
c(NO2)/mol·L-1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
(1)该反应的平衡常数表达式为________;从表中分析:
c1________c2,c3________c4(填“>”、“<”或“=”)。
(2)在上述条件下,从反应开始直至达到化学平衡时,N2O4的平均反应速率为________mol·L-1·s-1。
(3)达平衡后下列条件的改变可使NO2气体浓度增大的是________(填字母序号)。
A.扩大容器的容积
B.再充入一定量的N2O4
C.分离出一定量的NO2
D.再充入一定量的He
(4)若在相同条件下,起始时只充入0.080 mol NO2气体,则达到平衡时NO2气体的转化率为________。