题目内容
已知3Cu+8HNO3═3 Cu(NO3)2+2NO+4H2O
(1)该反应的还原产物是 .
(2)将化学方程式改写成离子方程式 .
若有6mole-发生转移,则
(3)被氧化的铜的物质的量为 .
(4)被还原的硝酸的质量是 .
(5)生成的NO在标准状况下的体积为 .
(6)已知硝酸溶液的体积为2L,硝酸全部参与反应,则该硝酸的物质的量浓度为 .
(1)该反应的还原产物是
(2)将化学方程式改写成离子方程式
若有6mole-发生转移,则
(3)被氧化的铜的物质的量为
(4)被还原的硝酸的质量是
(5)生成的NO在标准状况下的体积为
(6)已知硝酸溶液的体积为2L,硝酸全部参与反应,则该硝酸的物质的量浓度为
考点:氧化还原反应,硝酸的化学性质
专题:氧化还原反应专题,氮族元素
分析:该反应中Cu元素化合价由0价变为+2价、N元素化合价由+5价变为+2价,
(1)该反应中的氧化剂是硝酸,其对应产物是还原产物;
(2)写成离子方程式时,金属单质、气体、弱电解质写化学式,可溶性的强电解质写离子;
(3)根据Cu和转移电子之间的关系式计算;
(4)根据被还原的硝酸和转移电子之间的关系式计算;
(5)根据NO和转移电子之间的关系式计算;
(6)根据N原子守恒计算硝酸浓度.
(1)该反应中的氧化剂是硝酸,其对应产物是还原产物;
(2)写成离子方程式时,金属单质、气体、弱电解质写化学式,可溶性的强电解质写离子;
(3)根据Cu和转移电子之间的关系式计算;
(4)根据被还原的硝酸和转移电子之间的关系式计算;
(5)根据NO和转移电子之间的关系式计算;
(6)根据N原子守恒计算硝酸浓度.
解答:
解:该反应中Cu元素化合价由0价变为+2价、N元素化合价由+5价变为+2价,
(1)该反应中的氧化剂是硝酸,其对应产物NO是还原产物,故答案为:NO;
(2)写成离子方程式时,金属单质、气体、弱电解质写化学式,可溶性的强电解质写离子,其离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,故答案为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
(3)设被氧化Cu的物质的量为x,
3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O 转移电子
3mol 6mol
x 6mol
3mo:6mol=x:6mol
x=
=3mol
故答案为:3mol;
(4)设被还原的硝酸的物质的量为y,
3Cu+2HNO3(被还原)+6HNO3=3Cu(NO3)2+2NO↑+4H2O 转移电子
2mol 6mol
y 6mol
2mol:6mol=y:6mol
y=
=2mol,
被还原硝酸质量=2mol×63g/mol=126g,
故答案为:126g;
(5)设生成NO体积为z
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O 转移电子
44.8L 6mol
z 6mol
44.8L:6mol=z:6mol
z=
=44.8L,
故答案为:44.8L;
(6)根据N原子守恒得,消耗n(HNO3)=2n(Cu(NO3)2)+n(NO)=2×3mol+2mol=8mol,其物质的量浓度=
=4mol/L,
故答案为:4mol/L.
(1)该反应中的氧化剂是硝酸,其对应产物NO是还原产物,故答案为:NO;
(2)写成离子方程式时,金属单质、气体、弱电解质写化学式,可溶性的强电解质写离子,其离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,故答案为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
(3)设被氧化Cu的物质的量为x,
3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O 转移电子
3mol 6mol
x 6mol
3mo:6mol=x:6mol
x=
| 3mol×6mol |
| 6mol |
故答案为:3mol;
(4)设被还原的硝酸的物质的量为y,
3Cu+2HNO3(被还原)+6HNO3=3Cu(NO3)2+2NO↑+4H2O 转移电子
2mol 6mol
y 6mol
2mol:6mol=y:6mol
y=
| 2mol×6mol |
| 6mol |
被还原硝酸质量=2mol×63g/mol=126g,
故答案为:126g;
(5)设生成NO体积为z
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O 转移电子
44.8L 6mol
z 6mol
44.8L:6mol=z:6mol
z=
| 44.8L×6mol |
| 6mol |
故答案为:44.8L;
(6)根据N原子守恒得,消耗n(HNO3)=2n(Cu(NO3)2)+n(NO)=2×3mol+2mol=8mol,其物质的量浓度=
| 8mol |
| 2L |
故答案为:4mol/L.
点评:本题考查了物质的量的有关计算,根据方程式中各个物理量之间的关系式计算即可,注意该反应中硝酸的作用,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 马踏飞燕--是我国的旅游标志如图,出土的马踏飞燕是由表铜制成,下列有关该标志的叙述不正确的是( )
马踏飞燕--是我国的旅游标志如图,出土的马踏飞燕是由表铜制成,下列有关该标志的叙述不正确的是( )| A、青铜硬度比纯铜的硬度小 |
| B、青铜的主要成分是Cu、Sn、Pb等 |
| C、出土于东汉晚期 |
| D、青铜是我国使用最早的合金 |
下列表示不正确的是( )
| A、1 mol H2 |
| B、1 mol苹果 |
| C、1 mol N |
| D、1 mol H2SO4 |
下列化学方程式或离子方程式正确的是( )
| A、乙酸与碳酸钙固体反应的离子方程式:2H++CaCO3=Ca2++CO2↑+H2O |
B、苯酚钠溶液中通入少量二氧化碳的离子方程式: |
C、制备酚醛树脂的化学方程式: |
D、丙烯聚合成聚丙烯的化学方程式: |
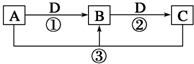 已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素.在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去).
已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素.在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去).