题目内容
12.甲烷分子是以碳原子为中心的正四面体结构,而不是正方形的平面结构,理由是( )| A. | 甲烷分子中的4个C-H键完全相等 | B. | CH3Cl 只有1种 | ||
| C. | CH2Cl2不存在同分异构体 | D. | CHCl3不存在同分异构体 |
分析 如果甲烷是正方形的平面结构,则CH2Cl2有两种结构:相邻或者对角线上的氢被Cl取代,而实际上,其二氯取代物只有一种结构,因此只有正四面体结构才符合,以此解答该题.
解答 解:A.甲烷无论是正四面体结构,还是正方形,四个键的键长、键角都相等,故A不选;
B.甲烷无论是正四面体结构,还是正方形,CH3Cl 均只有1种,故B不选;
C.若甲烷是正方形的平面结构,CH2Cl2有两种结构:相邻或者对角线上的氢被Cl取代,而实际上,其二氯取代物只有一种结构,因此只有正四面体结构才符合,故C选;
D.无论甲烷分子是以碳原子为中心的正四面体结构,还是平面正方形结构,CHCl3都不存在同分异构体,故D不选;
故选C.
点评 本题考查常见有机化合物的结构,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意CH2Cl2只代表一种物质,可以证明甲烷分子是空间正四面体结构,而不是平面正方形结构.

练习册系列答案
相关题目
3.R、X、Y、Z、W是短周期主族元素,它们在元素周期表中的相对位置如表所示.R最高价氧化物对应水化物与其简单气态氢化物反应可以形成离子化合物.下列推断正确的是( )
| R | X | Y |
| Z | W |
| A. | 最简单气态氢化物的热稳定性由强到弱的排序:Z、R、X、Y | |
| B. | R、X、Y、Z、W各元素最高价和最低价的绝对值之和均为8 | |
| C. | 最高价氧化物的水化物酸性由弱到强的排Z、R、W | |
| D. | RY3、W2X、ZW5分子中每个原子最外层都达到8 电子结构 |
20.抗疟特效药青篙素最早是从黄篙中提取出来的,化学家在青篙素的基础上又合成了疗效更好的双氢青篙素.从青篙素的发现到双氢青篙素的应用,下列工作:
①提取青篙素;
②研究青篙素的分子组成及结构;
③研究青篙素的合成方法,并不断改进合成路线;
④适当改变青篙素的结构以使其药效更好.
其中化学工作者必须做的有( )
①提取青篙素;
②研究青篙素的分子组成及结构;
③研究青篙素的合成方法,并不断改进合成路线;
④适当改变青篙素的结构以使其药效更好.
其中化学工作者必须做的有( )
| A. | ①② | B. | ①②③ | C. | ②③④ | D. | ①②③④ |
7.下列反应中△H>0,△S>0的是( )
| A. | 2Mg(s)+CO2(g)→2MgO(s)+C(s) | |
| B. | 低温下能自发进行的反应:NH3(g)+HCl(g)→NH4Cl(s) | |
| C. | 高温下能自发进行的反应:SiO2(s)+2C(s)→Si(s)+2CO(g) | |
| D. | 任何温度下均能自发进行的反应:2H2O2(l)→2H2O(l)+O2(g) |
4.下列离子方程式正确的是( )
| A. | 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+ | |
| B. | 铜作电极电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- | |
| C. | 用白醋除铁锈:Fe2O3+6H+═3H2O+2Fe3+ | |
| D. | HCO3-水解:HCO3-+H2O?CO32-+H3O+ |
3.下列化学用语表达错误的是( )
| A. | 1-丁烯的键线式: | B. | 乙醛的填充模型: | ||
| C. | 羟基的电子式: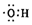 | D. | 葡萄糖的结构简式:C6H12O6 |